Introduction
자동차 타이어는 천연고무(natural rubber, NR), 스타이렌-부타디엔 고무(styrene-butadiene rubber, SBR), 그리고 부타디엔 고무(polybutadiene rubber, BR)를 사용하여 제조한다.1 승용차용 타이어 트레드 고무는 주로 SBR과 BR을 혼합하여 제조한다.2 BR은 타이어 트레드의 내마모성을 향상시킨다. 2가지 이상의 고무가 혼합된 블렌드 고무 배합물의 경우 혼합된 고무 비율에 따라 화학적 특성과 물리적 특성이 다르게 나타난다.1 따라서, 블렌드 고무의 함량비를 분석하는 것이 중요하다.
블렌드 고무의 함량비 분석에는 푸리에 변환-적외선 분광법(Fourier transform infrared spectroscopy, FT-IR), 핵자기공명분석법(nuclear magnetic resonance spectroscopy, NMR), 열중량분석법(thermogravimetric analysis, TGA), 시차주사열량분석법(differential scanning calorimetry, DSC), 열분해-기체 크로마토그래피/질량분석법(pyrolysis-gas chromatography/mass spectrometry, Py-GC/MS) 등이 사용된다.1,3,4 NMR을 이용하여 SBR의 미세구조를 분석하기 위해서 원재료 고무를 CDCl3에 용해시킨 후 1H-NMR로 분석한다.3 IR 분석을 위해서 고무 용액을 KBr window에 코팅 후 투과 방식으로 분석한다. NMR과 IR은 분석 전 가교된 고무 시료에서 가교 결합을 끊고 고분자 성분을 추출하는 시료 전처리 과정이 필요하다. 고무 조성비를 정량하기 위해서 열분해기가 장착된 FT-IR을 사용할 수 있다.4 699 cm−1와 967 cm−1로 각각 SBR과 BR의 함량을 계산한다. 699 cm−1은 styrene에 의해 나타나고 967 cm−1은 trans-1,4-unit butadiene에서 나타난다. 하지만 해당 피크는 배음과 조합에 의한 피크가 나타나는 파수 영역으로 미지의 블렌드 고무에서는 식별이 곤란하다. TGA 분석은 SBR과 BR의 유사한 열분해 거동으로 인해 정량 분석이 곤란하다.4 DSC를 이용하여 고무 조성비를 결정할 때는 유리 전이 온도(glass transition temperature, Tg)를 사용한다.4NR/SBR이나 NR/BR 블렌드 고무와는 달리 SBR/BR 블렌드 고무는 Tg 차이가 크지 않아 함량비를 분석하기 곤란하다.
Yang 등은 Py-GC/MS로 혼합 고무의 함량을 분석하기 위해서 카본블랙이 포함되지 않은 고무 블렌드를 이용하여 SBR/BR 고무에서 SBR의 함량에 따른 열분해 생성물의 피크면적비를 도식하여 검량선을 작성하였다.1 분석에 사용한 고무는 가교 구조를 끊기 위해 과산화수소와 사이클로헥산으로 고무를 용해시켰다. SBR과 BR을 식별할 열분해생성물로 4-vinylcyclohexene (VCH)와 styrene을 이용하였다. 이때 열분해 생성물의 피크면적비는 styrene/(styrene + VCH) 피크면적비로 계산하였다.
블렌드 고무 제품의 고무 성분비를 분석하기 위해서는 고무 조성을 변화시킨 검량선 작성이 필요하다. 검량선 작성에 사용하는 표준시료로는 분석 대상과 동일한(혹은 거의 유사한) 배합사양을 갖는 가황물 시험편을 제조하여 사용하는 것이 가장 바람직하지만, 가황 고무 제조에는 시간과 비용이 요구되며, 더군다나 미지 시료인 경우에는 정확한 배합사양을 알 수 없으므로 다른 방법의 개발이 필요하다. 본 연구에서는 SBR/BR 고무 배합물의 조성비를 정량하기 위해 원재료 고무를 이용하여 검량선을 작성하였다. 원재료 고무 용액을 사용하여 표준시료를 제조하였으며, 이를 이용하여 Py-GC/MS 분석에 대한 검량선을 작성하였다. 고무 용액은 SBR/BR 혼합용액을 만들거나 SBR과 BR 용액을 따로 제조하여 조성비에 따라 혼합하여 표준시료를 제조하여 사용하였다. 고무 용액을 이용한 표준시료의 검량선과 별도로 제조한 가황 고무를 이용한 표준시료의 검량선을 비교하였다. 실험 오차를 줄이기 위해 모든 분석에서 고무 양은 일정하게 유지하였다.
Experimental
SBR과 BR의 용액 제조를 위해 SBR1502 (금호석유화학)와 BR01 (금호석유화학)을 사용하였다. 용매로는 톨루엔(J. T. Baker, USA)을 사용하였다. SBR과 BR의 혼합 비율을 100/0, 90/10, 80/20, 60/40으로 설정하였다. 시료는 3가지 방법으로 준비하였다. 용액을 이용한 시료 준비 절차를 Figure 1에 나타냈다. Figure 1(A)는 SBR과 BR의 혼합 비에 따라 제조한 혼합용액을 사용한 표준시료인 ‘시료(Mix)’의 준비 절차이다. 혼합 용액 1 μL에 고무 10 μg이 포함되도록 용액(10 mg/mL)을 제조하였다. 혼합 용액 5 μL (50 μg에 해당)를 마이크로 피펫을 이용하여 슬라이드 글라스에 떨구었다. 용매를 제거하기 위해 70°C 오븐에서 30분 동안 건조시킨 후 칼을 이용하여 건조된 고무를 긁어 모았다. Figure 1(B)는 SBR과 BR의 개별 용액을 제조하여 혼합 비율에 맞춰 섞어 제조한 표준시료인 ‘시료(Each)’의 준비 절차이다. 이때 얻어지는 SBR과 BR의 혼합 고무의 무게가 50 μg이 되도록 용액을 제조하였다. 슬라이드 글라스에 혼합비에 맞게 먼저 SBR 용액을 떨군 후 70°C 오븐에서 30분 동안 건조하여 용매를 제거하였다. 건조된 SBR 필름 위에 혼합 비율대로 BR 용액을 떨구고 70°C 오븐에서 30분 동안 건조하였다. 건조 후에는 칼로 고무를 긁어 모았다. 세번째 시료는 SBR1502와 BR01을 이용하여 배합한 고무 가황물을 표준시료로 사용한 ‘시료(Vul)’이다. 설정한 SBR/BR 혼합비에 따라 배합된 고무 가황물에서 고무가 약 50 μg이 포함되는 가황물의 무게를 계산하고 잘라서 분석에 이용하였다. 고무 가황물은 고무 이외에 충전제 60 phr, 총 유기물 20 phr, 산화아연 4 phr을 포함하고 있다. TBBS 2 phr과 황 1.5 phr을 사용하였다.

열분해 분석을 위해 CDS Pyroprobe 1500 (CDS Analytical Inc.) 열분해 장치를 GC/MS에 연결하여 사용하였다. 열분해는 250°C에서 15 초간 예열 후 590°C에서 10 초간 진행하 였다. Agilent 사의 6890 GC에 Agilent 사의 5973 MS를 장착하여 사용하였다. 컬럼은 DB-5MS (길이 30 m, 내경 0.32 mm, 필름 두께 0.25 μm, Agilent Technology Inc.)를 사용하였다. 시료 주입구 온도는 250°C, 분할비는 1 : 15이며, 이동상 기체는 헬륨(1.8 mL/min)을 사용하였다. 컬럼 오븐의 온도 프로그래밍은 30°C에서 3.0분간 유지 후, 8 °C/min의 속도로 160°C까지 올려 1.0분간 유지하였고, 10°C/min의 속도로 250°C까지 올려 3.0분간 유지하였다. 분석물의 이온화에는 전자 이온화(electron ionization)를 이용하였고 MS source 온도는 230°C로 설정하였다. 동일 시료를 3회 분석하여 평균하였다.
Results and Discussion
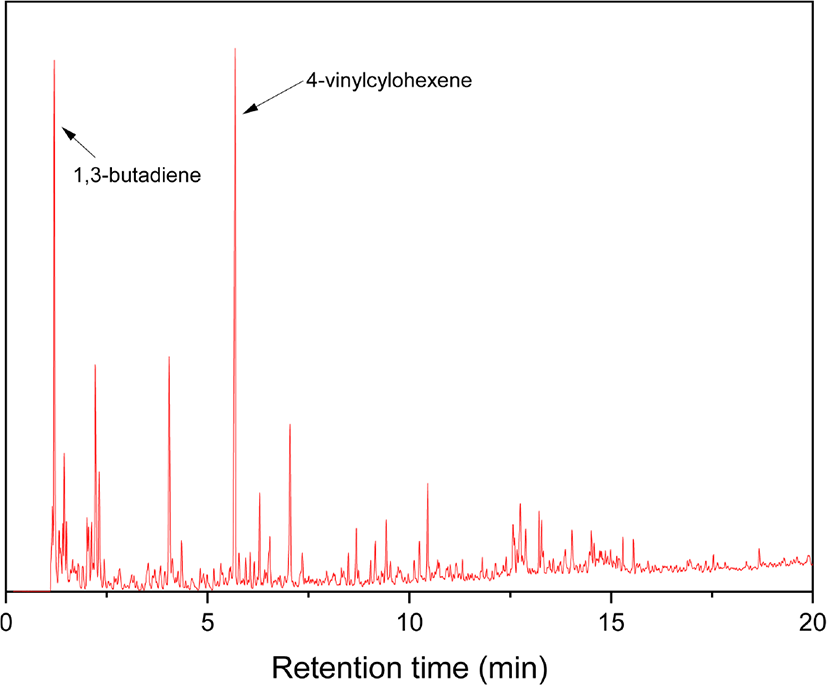
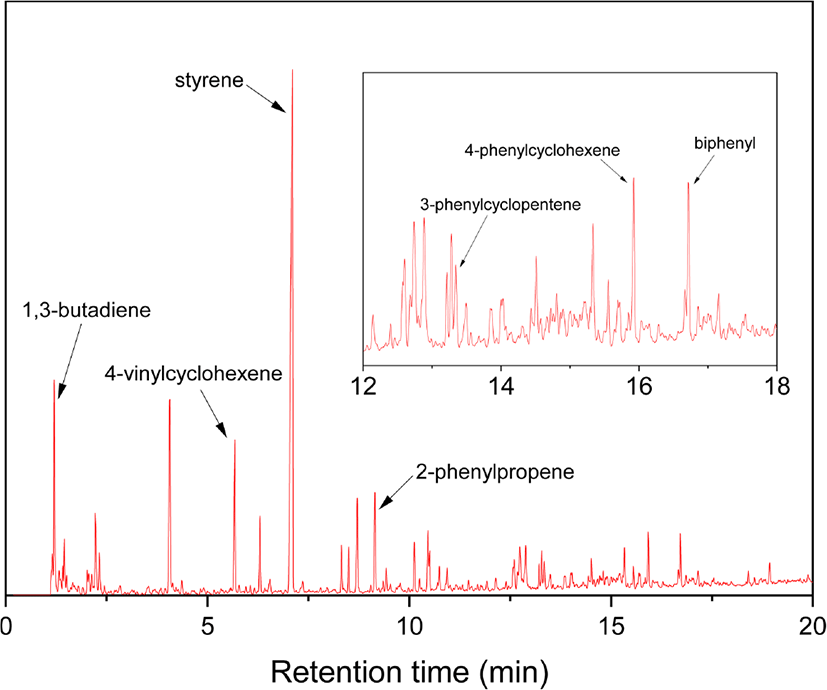
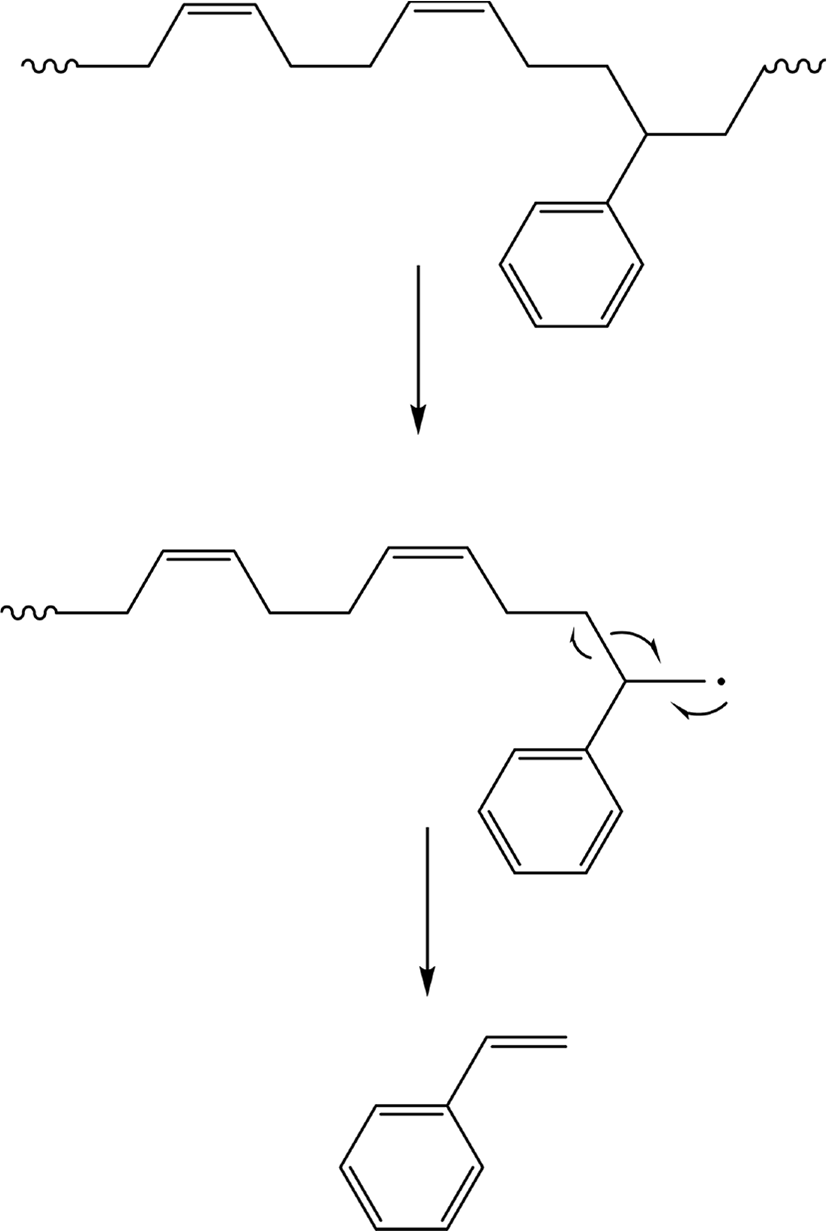
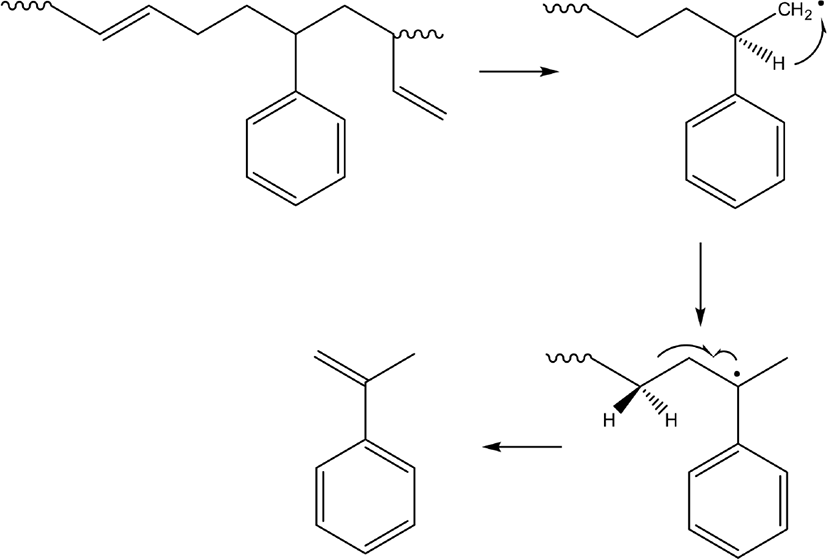
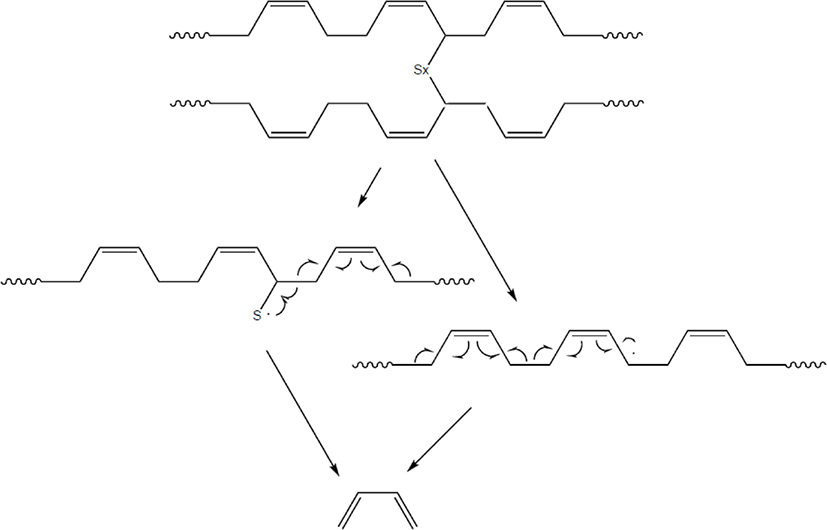
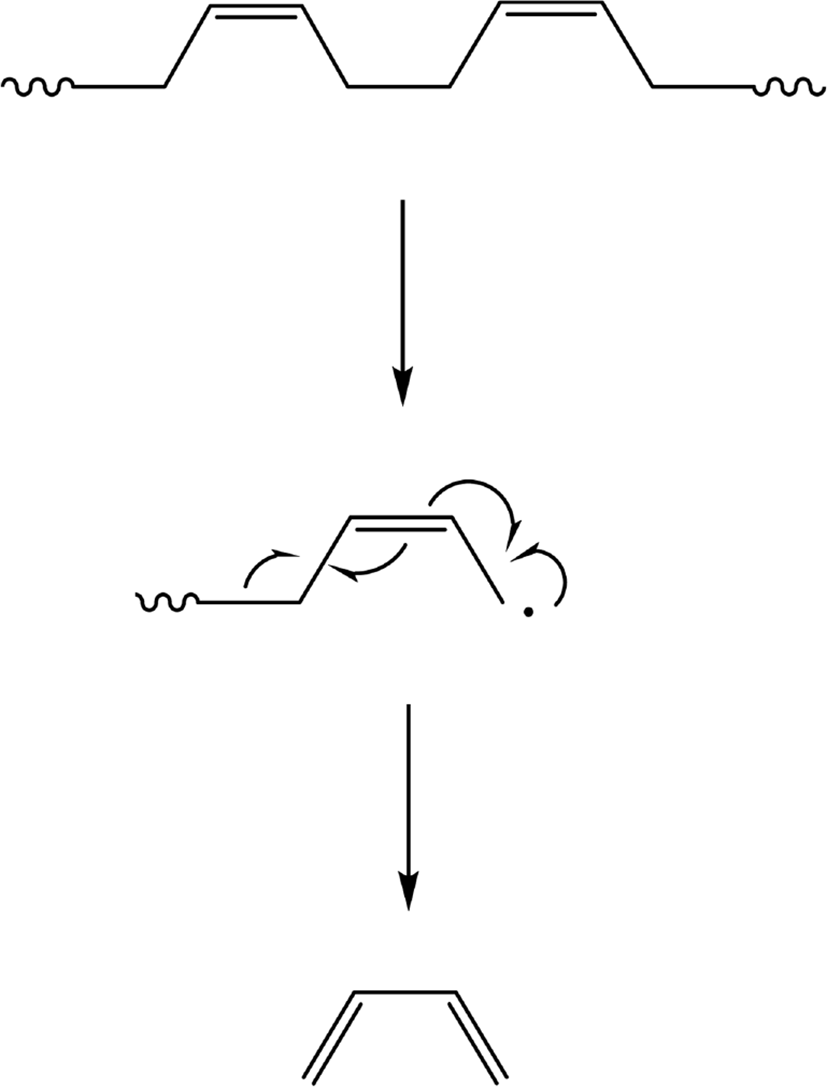
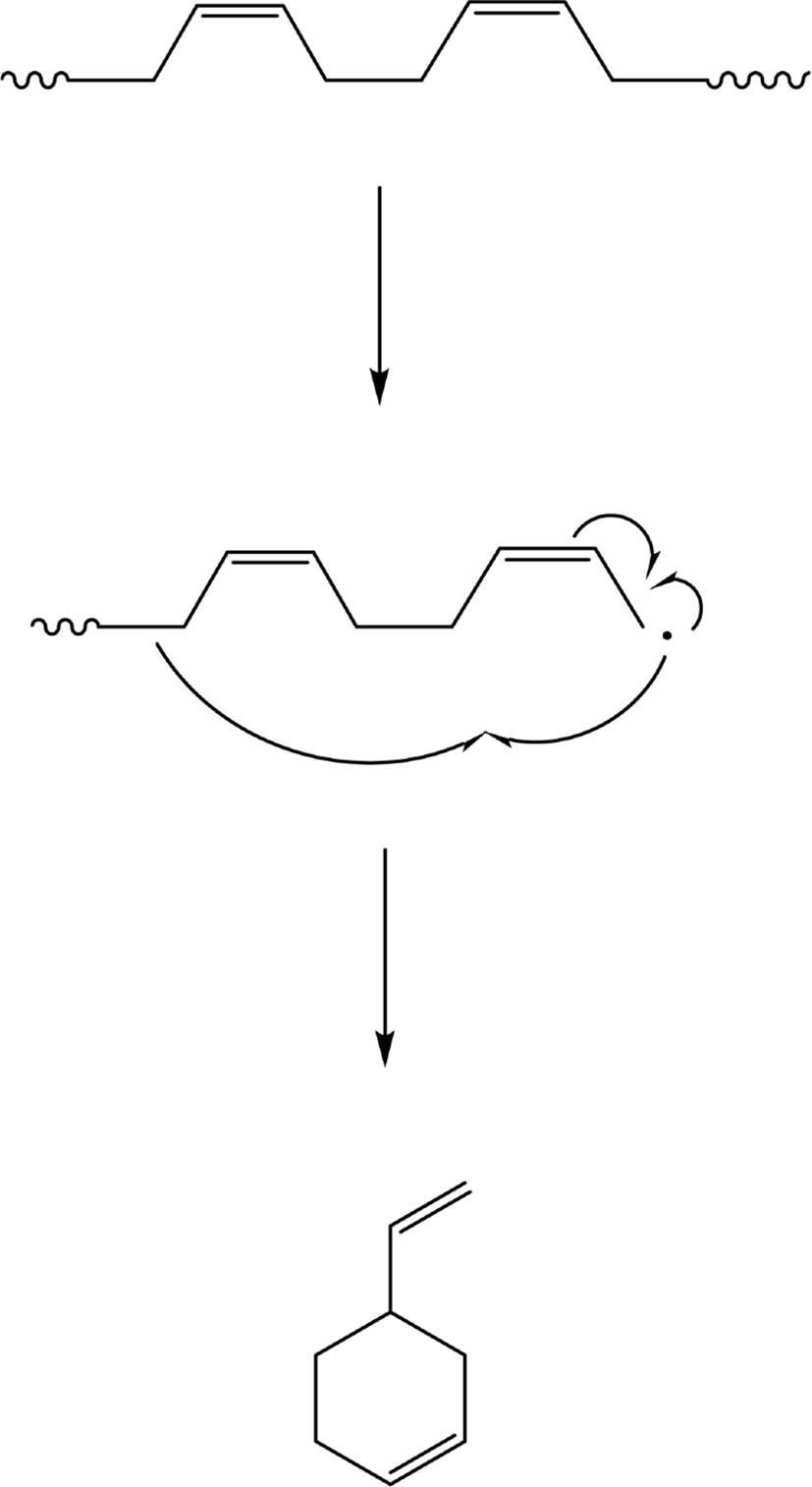
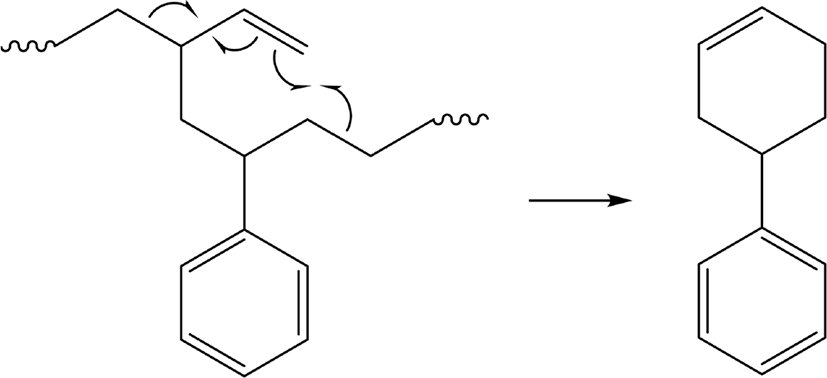
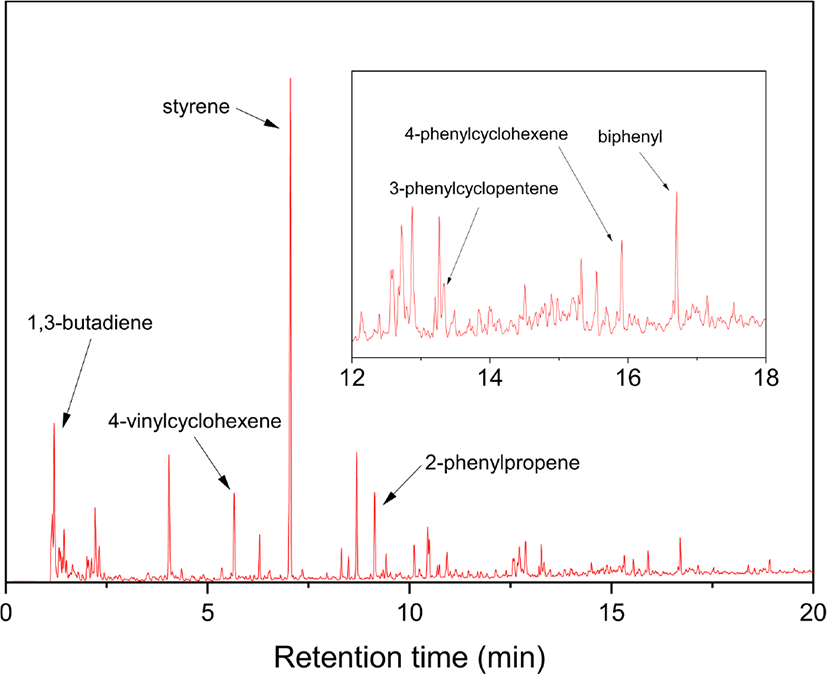
Figure 2에 SBR 용액으로 제조한 시료(Each) (SBR solution)와 원재료 SBR (SBR particle), 그리고 가황 SBR (SBR vulcanizate, 시료(Vul))의 확대 사진을 제시하였다. 모두 고무 무게 50 μg에 해당한다. Figure 3은 BR의 Py-GC/MS 크로마토그램으로 주요 열분해생성물로 butadiene과 4-vinylcyclohexene (VCH)의 검출은 BR의 존재를 의미한다. Butadiene과 VCH가 BR이나 SBR의 butadiene sequence의 열분해에 의해 생성되는 메커니즘을 각각 Scheme 1과 2에 나타내었다. Figure 4는 SBR의 Py-GC/MS 크로마토그램으로 다양한 열분해생성물을 볼 수 있다. Styrene은 SBR의 styrene 단량체에서 생성되는 것으로, styrene의 열분해 생성 메커니즘을 Scheme 3에 나타내었다. Butadiene과 VCH는 BR의 존재와 더불어 SBR의 butadiene sequence의 존재를 알려주는 주요 열분해생성물이다. 2-Phenylpropene (PhP), 2-phenylcyclopentene (PhCP), 4-phenylcyclohexene (PhCH)은 styrene-butadiene sequence의 열분해에 의해 생성되는 것으로 이들의 검출로 SBR임을 확인할 수 있다. SBR에서 PhP와 PhCH가 열분해되어 생성되는 메커니즘을 각각 Scheme 4와 5에 나타내었다. Figure 5는 SBR/BR 블렌드의 Py-GC/MS 크로마토그램으로 다양한 열분해생성물이 나타났으며 SBR = 100의 Py-GC/MS 크로마토그램과 큰 차이가 없으나, 상대적으로 PhP, PhCP, PhCH가 적게 검출된 것을 알 수 있다.
SBR과 BR의 대표적 열분해생성물은 각각 styrene과 butadiene이라 할 수 있다. Figure 6은 SBR/BR 블렌드의 열분해생성물 중 butadiene과 styrene 비율(1,3-butadiene/styrene)을 BR 함량에 따라 도식한 결과이다. 시료(Vul)의 1,3-butadiene/styrene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)에서보다 월등히 크게 나타났다. 심지어 SBR = 100에서도 월등히 크게 나타났다. 그 이유는 황 가교의 분해 때문으로 해석할 수 있다. 황 가교는 SBR에서 butadiene 단량체의 탄소-탄소 이중결합(~C=C~) 옆의 알릴 수소(allylic hydrogen)에서 주로 형성되며 황 가교(~S-C~, ~S-S~)는 SBR 주쇄인 탄소-탄소 단일 결합(~C-C~)보다 약하므로 열에 의해 우선적으로 분해된다. 따라서 황 가교의 분해에 의해 butadiene 단량체 부분에서 형성된 생성을 촉진시킨다(Scheme 6).5
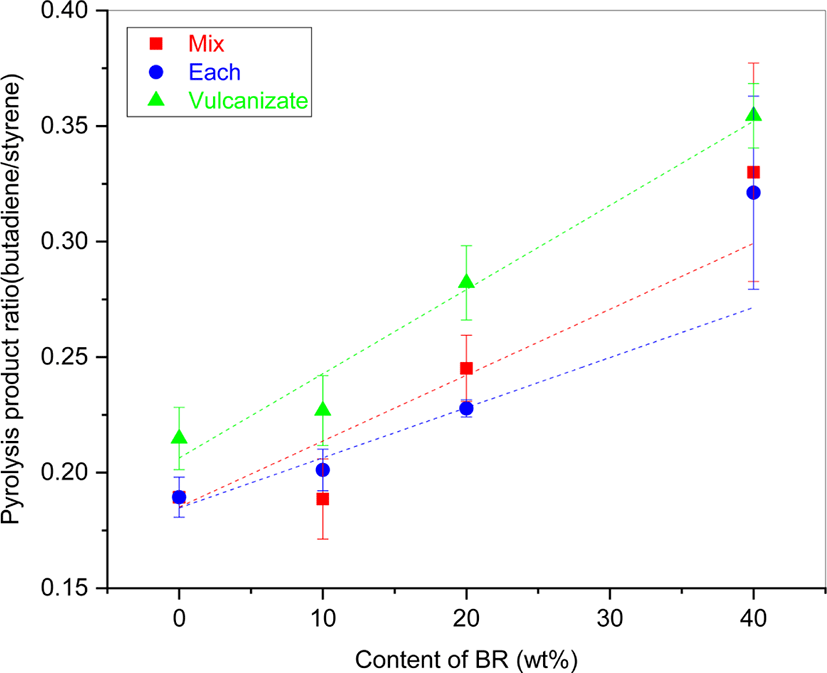
시료(Mix)의 1,3-butadiene/styrene 비율이 시료(Each)보다 더 크게 나타났다. 시료(Mix)는 분자 수준으로 완전히 혼합된 것으로 볼 수 있으며, 시료(Each)는 덜 혼합되어 일부 혹은 대부분이 각각의 영역으로 존재할 것이다. 이러한 시료의 상태가 열분해생성물의 생성비의 차이로 나타나는 것으로 해석할 수 있다. 상대적으로 양이 많은 SBR 위에 BR 용액을 더하여 고무 시료를 긁어 모았으므로, 시료(Each)의 외부에는 상대적으로 SBR이 더 많이 존재하고 시료 내부보다는 외부에 열이 좀더 효율적으로 전달되었을 것으로 여겨진다. 따라서 SBR에서 생성되는 styrene이 BR에서 생성되는 butadiene보다 양이 더 많을 것이다. 시료(Mix)의 기울기가 시료(Vul)의 기울기와 유사하므로 원재료 고무 용액을 이용한 검량선 작성에는 시료(Each)보다는 시료(Mix)를 사용하는 것이 보다 적절하다고 할 수 있다. Table 1에 Figure 6과 7의 곡선 접합(curve fitting)에 의해 얻은 일차방정식과 상관계수(R2)를 정리하였다. Butadiene/styrene 비의 변화 도식에서는 시료(Vul)가 우수한 상관성을 보였으나 시료(Mix)의 상관성은 그다지 높지 않았다.
Figure 7은 SBR/BR 블렌드의 열분해생성물 중 butadiene dimer인 VCH와 styrene 비율(VCH/styrene)을 BR 함량에 따라 도식한 결과이다. 시료(Vul)의 VCH/styrene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)보다 월등히 작게 나타났으며, 심지어 SBR = 100에서도 월등히 작게 나타났다. 그 이유는 황 가교의 영향으로 해석할 수 있다. 황 가교에 의해 자유로운 butadiene sequence의 길이가 짧아져서 butadiene dimer인 VCH의 형성이 제약을 받는다. 시료(Mix)의 VCH/styrene 비율이 시료(Each)보다 더 작게 나타났다. SBR에서는 styrene 단량체로 인해 butadiene sequence의 길이가 제약을 받아 BR에 비해 VCH의 생성이 줄어든다. VCH의 생성은 butadiene의 생성보다 상대적으로 낮은 열분해온도에서 유리하기 때문에,6,7 SBR이 BR을 일부분 감싸고 있는 형태인 시료(Each)에서 VCH의 생성이 더 유리할 것으로 여겨진다. 시료(Vul)의 VCH/styrene 비율 변화에 대한 검량선의 상관성은 보통으로 보이나 실제 데이터와 직선식의 관계가 매우 좋지 않고 오차 범위가 커서 고무 용액을 이용한 표준시료의 검량선으로 이를 대체하기는 곤란할 것으로 판단된다.
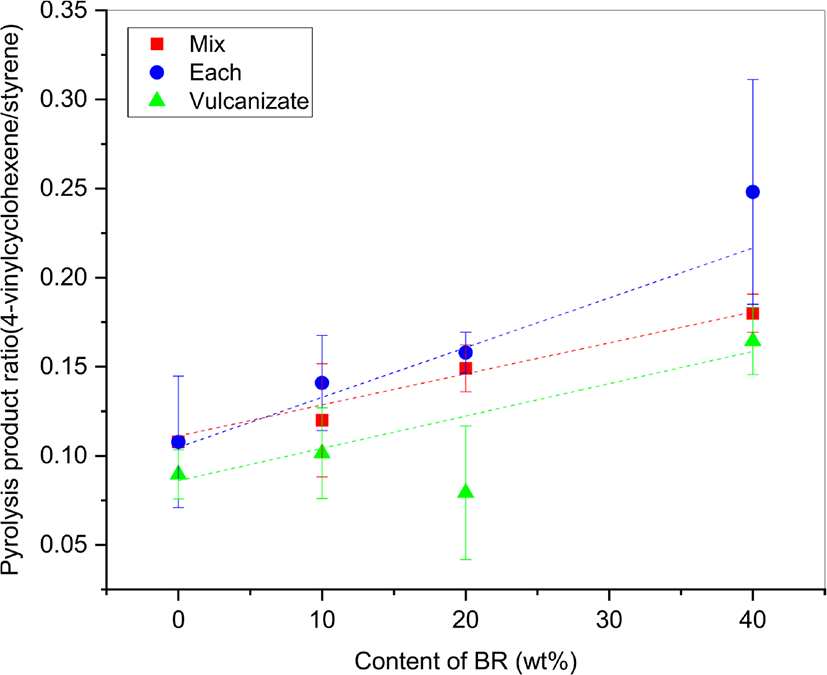
Figure 8은 SBR/BR 블렌드의 열분해생성물 중 styrene-butadiene sequence에서 생성되는 PhP와 butadiene 비율(PhP/butadiene)을 BR 함량에 따라 도식한 결과이다. Butadiene/styrene 변화 도식이나 VCH/styrene 변화 도식과 달리 BR이 증가할수록 감소하는 경향을 보인다. 시료(Vul)의 PhP/butadiene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)에서보다 월등히 작게 나타났으며, 심지어 SBR = 100에서도 작게 나타났다. 그 이유는 황 가교의 영향으로 해석할 수 있다. 앞서 설명하였듯이 황 가교의 분해에 의해 butadiene 생성이 활성화되기 때문이다. 시료(Each)의 경우 PhP/butadiene 비율이 BR 함량에 따라 거의 변화가 없으므로 시료(Each)는 검량선의 표준시료로 사용할 수 없다. 반면, 시료(Mix)의 기울기는 시료(Vul)와 유사하므로 이를 대체할 수 있을 것이다.
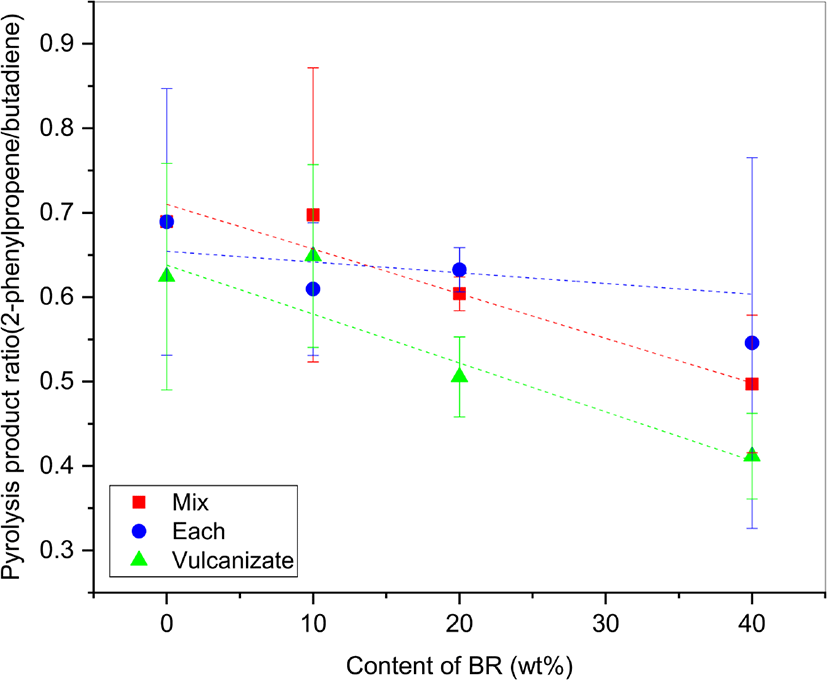
Figure 9는 SBR/BR 블렌드의 열분해생성물 중 styrene-butadiene sequence에서 생성되는 PhCH와 butadiene 비율(PhCH/butadiene)을 BR 함량에 따라 도식한 결과이다. PhP/butadiene 도식과 마찬가지로 BR이 증가할수록 감소하는 경향을 보인다. 시료(Vul)의 PhCH/butadiene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)보다 작게 나타났으며, 심지어 SBR = 100에서도 작게 나타났다. 그 이유는 황 가교의 영향으로 해석할 수 있다. 앞서 설명하였듯이 황 가교의 분해에 의해 butadiene의 형성이 활성화되기 때문이다. 시료(Vul), 시료(Mix), 시료(Each)의 검량선이 유사하지만, 시료(Vul)의 오차 범위가 너무 넓어 검량선으로 사용하기에는 적합하지 않다.
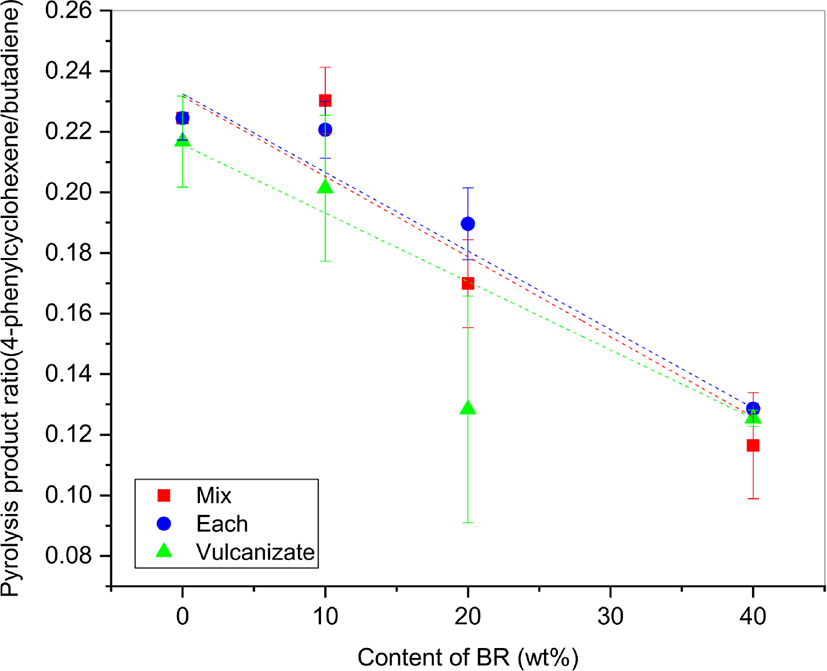
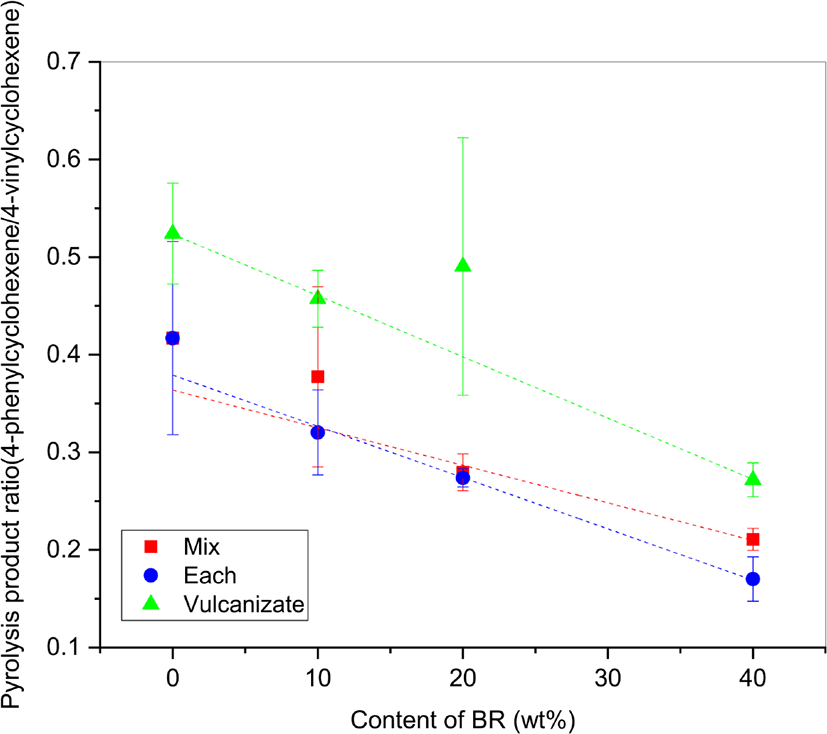
Figure 10과 11은 각각 BR 함량에 따른 PhP/VCH와 PhCH/VCH 변화에 대한 도식이다. 모두 시료(Vul)의 값이 원재료 고무 용액으로 제조한 표준시료인 시료(Mix)와 시료(Each)의 값보다 크게 나타났는데, 그 이유는 황 가교로 인해 VCH의 생성이 줄어들었기 때문이다. 시료(Vul)의 상관성이 낮거나 오차 범위가 커서 용액으로 제조한 표준시료로 대체하여 검량선으로 사용하기는 곤란하다.
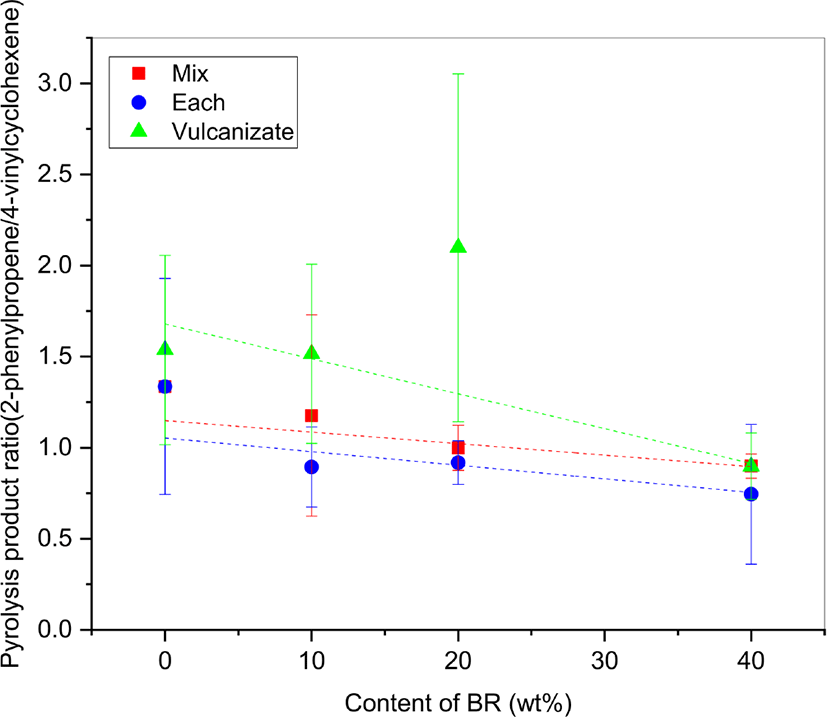
Table 2에 Figure 8, 9, 10, 11의 곡선 접합에 의해 얻은 일차방정식과 상관계수(R2)를 정리하였다. PhP/butadiene 비의 변화 도식에서는 시료(Vul)의 상관성은 보통이나 시료(Mix)의 상관성은 매우 우수하게 나타났다. 또한, 시료(Vul)와 시료(Mix)의 기울기는 각각 5.29×10−3과 5.80×10−3으로 그 차이는 10% 미만으로 작게 나타났다. 하지만 PhCH/butadiene과 PhCH/VCH 비의 변화 도식에 대한 시료(Vul)의 상관성은 우수하게 나타났으나 오차 범위가 매우 커 검량선으로 사용하기에는 적절하지 않다.
Conclusions
BR과 SBR의 열분해생성물 중 SBR/BR 블렌드 고무배합물에서 SBR과 BR의 함량비를 분석하기 위한 검량선 지표로 1,3-butadiene/styrene, VCH/styrene, PhP/butadiene, PhP/VCH, PhCH/butadiene, PhCH/VCH의 변화를 검토한 결과, 혼합한 SBR/BR 용액을 이용하여 작성한 검량선 중 1,3-butadiene/styrene과 PhP/butadiene을 가황물 대신 사용이 가능한 것으로 나타났다. 1,3-Butadiene/styrene 비율은 BR 함량이 높아질수록 증가한다. 시료(Vul)의 1,3-butadiene/styrene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)에서보다 월등히 크게 나타났는데, 그 이유는 황 가교의 분해로 butadiene의 생성이 촉진되기 때문이다. 시료(Mix)의 1,3-butadiene/styrene 비율이 시료(Each)보다 더 크게 나타났는데, 시료(Mix)는 분자 수준으로 완전히 혼합되었으나 시료(Each)의 외부에는 상대적으로 SBR이 많아 열이 좀더 효율적으로 전달되었기 때문으로 해석할 수 있다. 1,3-Butadiene/styrene 비율 변화 도식에 대한 시료(Mix)의 기울기가 시료(Vul)의 기울기와 유사하므로 원재료 고무 용액을 이용한 검량선 작성에는 시료(Each)보다는 시료(Mix)를 사용하는 것이 보다 적절하다고 할 수 있다. PhP/butadiene 변화 도식은 BR이 증가할수록 감소하는 경향을 보였다. 시료(Vul)의 PhP/butadiene 비율이 용액을 사용하여 제조한 시료(Mix)와 시료(Each)보다 월등히 작게 나타났으며 심지어 SBR = 100에서도 작게 나타났는데, 그 이유도 마찬가지로 황 가교에 의해 butadiene 생성이 활성화되었기 때문이다. 시료(Each)의 경우 PhP/butadiene 비율이 BR 함량에 따라 거의 변화가 없으므로 시료(Each)는 검량선의 표준시료로 사용할 수 없는 반면, 시료(Mix)의 기울기는 시료(Vul)와 유사하므로 이를 대체할 수 있을 것이다.