Article
Analytical Method for Determination of Microstructure of SBR and SBR Content in Blended Rubber Composites Using Pyrolytic Technique
Eunji Chae1, Sung-Seen Choi1,†
Author Information & Copyright ▼
1Department of Chemistry, Sejong University, 209 Neungdong-ro, Gwangjin-gu, Seoul 05006, Republic of Korea
© Copyright 2022 The Rubber Society of Korea. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Nov 28, 2022; Revised: Dec 01, 2022; Accepted: Dec 03, 2022
Published Online: Dec 31, 2022
Abstract
Styrene-butadiene rubber(SBR) is a copolymer of styrene and butadiene. It is composed of 1,2-unit, 1,4-unit, and styrene, and its properties are dependent on its microstructure. In general, rubber composites contain a single rubber or a blended rubber. Similarly, SBR is used by mixing with natural rubber(NR) and butadiene rubber(BR). The composition of a rubber article affects its physical and chemical properties. Herein, an analytical method for determining the microstructure of SBR using via pyrolysis is introduced. Pyrolysis-gas chromatography/mass spectrometry is widely used to analyze the microstructure of polymeric materials. The microstructure of SBR can be determined by analyzing the principal pyrolysis products formed from SBR, such as 4-vinylcyclohexene, styrene, 2-phenylpropene, 3-phenylcyclopentene, and 4-phenylcyclohexene. An analytical method for determining the composition of SBR/NR, SBR/BR, and SBR/NR/BR blends via pyrolysis is introduced. The composition of blended rubber can be determined by analyzing the principal pyrolysis products formed from each rubber component.
Keywords: pyrolysis-gas chromatography/mass spectrometry; styrene-butadiene rubber; microstructural analysis; natural rubber; butadiene rubber
Introduction
Styrene-butadiene rubber(SBR)은 가장 널리 사용하는 합성 고무 중 하나로 styrene과 butadiene의 공중합체이다.1-7 BR과 SBR에서 butadiene sequence는 1,2-unit과 1,4-unit으로 나뉘어지며, 1,4-unit은 다시 cis-1,4-unit과 trans-1,4-unit으로 구별한다.2 SBR의 특성은 이들 4가지 미세구조 성분의 비율에 따라 달라진다. SBR은 합성방법에 따라 유화중합 SBR(emulsion SBR, ESBR)과 용액중합 SBR(solution SBR, SSBR)로 구분된다. 용액중합은 미세구조 조정이 가능하여 SSBR은 ESBR보다 더 복잡한 미세구조를 가지고 있으며 일반적으로 SSBR은 1,2-unit 함량이 높은 경향이 있다. SSBR은 보통 ESBR보다 좁은 분자량 분포를 갖는다.3
SBR의 미세구조는 탄성체들의 물리적 특성에 영향을 미친다. SBR의 미세구조에 따라 고무와 충진제 사이의 상호작용이 달라진다.8 고무 탄성체의 물리적 특성은 가교밀도에 의해서도 달라진다.9,10 황 가교 SBR에서 가교밀도의 변화는 1,2-unit의 함량이 증가함에 따라 감소하는 경향을 보인다.11 SBR은 호스, 신발 등의 다양한 소재로 이용되며 승용차용 타이어 트레드 제조에 많이 사용된다.1,2 일반적으로 SBR을 단독으로 사용하는 것보다 NR 혹은 BR과 혼합하여 사용하는 경우가 많다.
SBR의 미세구조는 적외선분광법(infrared spectroscopy, IR)과 핵자기공명분광법(nuclear magnetic resonance spectroscopy, NMR)과 같은 분광학적 방법과 열분해 분석법을 이용하여 분석할 수 있다. SBR은 IR 분석을 통해 styrene, 1,2-unit, cis-1,4-unit, trans-1,4-unit의 함량을 결정할 수 있다.12-17 NMR 분석을 통해 styrene, 1,2-unit, 1,4-unit의 함량을 결정할 수 있다.6,7 특히, IR 분광법은 cis-1,4-unit의 함량을 결정할 수 있다는 장점이 있다. 하지만 두 방법은 분석을 위해 고무만을 추출해야 좋은 분석 결과를 얻을 수 있다.1,5,18
본 논문에서는 SBR의 미세구조와 SBR이 포함된 블렌드 고무의 조성을 열분해-기체 크로마토그래피/질량분석법(pyrolysis-gas chromatography/mass spectrometry, Py-GC/MS)을 사용하여 분석하는 방법을 정리하여 소개하였다. 또한, 열분해 장치의 종류와 특성에 대해서도 소개하였다. Py-GC/MS는 열분해 장치에서 생성된 열분해생성물을 GC에 바로 주입하여 개개의 성분으로 분리하고, 분리된 각 성분을 질량분석기로 정성 및 정량 분석하는 방법이다. Py-GC/MS는 고체 시료 그대로 분석 가능하기 때문에 분광학적 방법에 비해 시료 전처리 과정이 없다는 장점이 있다.19-22
Pyrolysis Methods
1. Furnace type pyrolyzer
회화로(furnace) 열분해기는 순간(flash) 열분해와 천천히 온도를 올리는 열분해가 모두 가능하다.23 순간 열분해의 원리는 회화로를 원하는 열분해 온도로 유지하고 시료를 회화로에 넣는 것이다. 일반적으로 GC의 이동상으로 사용하는 헬륨과 같은 비활성기체의 흐름은 가열로를 통과하여 열분해생성물을 이동시킨다. 회화로 열분해기는 수평형과 수직형이 있다.24 수평형 장치에서 시료는 열분해 온도가 미리 설정된 회화로에 수동으로 삽입되는 시료 보트에 놓인 후 열분해가 진행된다. 하지만 수평형 회화로 열분해기는 시료 보트의 높은 열용량과 큰 불용체적(dead volume)으로 인해 거의 사용되지 않는다. 효율적인 열분해를 위해서 낮은 불용체적을 갖는 작은 회화로가 사용된다.23 최근에는 시료를 저온 구역에서 가열 구역으로 떨어뜨리는 수직형 마이크로 회화로가 많이 사용되고 있다.23-25 마이크로 회화로는 가열 장치 내에 속이 빈 석영관이 있고, 시료가 담긴 컵은 중력에 의해 자유 낙하되어 수직 회화로의 중앙으로 떨어진다.23,24 시료 컵 이외에도 액체 주사기나 고체 플런저(plunger) 주사기를 사용하여 시료를 주입할 수 있다.26,27 회화로 방식은 다양한 온도에서 열분해 시킬 수 있으며1 °C 간격으로 800 °C까지 프로그래밍도 가능하다.18,24 승온 속도는 1-100 °C/min까지 조절 가능하며 회화로에 시료가 떨어지고 0.1초 이내에 열분해 온도에 도달한다.
2. Filament pyrolyzer
필라멘트(filament) 열분해기는 원하는 열분해 온도에 도달하기 위해 코일 혹은 리본 필라멘트에 전류를 흘려 시료에 열이 가해지는 방식이다.23 백금과 같은 저항성 금속이 필라멘트로 사용되며 코일이나 리본 형태의 프로브(probe)를 사용한다.24-27 코일에는 시료가 포함된 작은 석영관이 삽입된다.23-25 시료가 들어 있는 석영관 주위를 직접 감싸고 있는 필라멘트는 열분해 장치 하우징(housing)에 배치되고 응축을 막기 위해 가열된다.23 휘발성 용매에 용해되는 시료는 리본 프로브를 사용할 수 있다.26 필라멘트 열분해기는 20 °C/ms의 가열 속도로 최대 1100 °C의 온도까지 도달할 수 있으며, 1 °C 간격으로 1400 °C까지 프로그래밍 가능하다.23,27,28 설정한 온도까지 15-50 ms 내에 도달한다.29 코일 프로브에서 실제 열분해 온도는 시료의 형상, 형태, 크기, 석영관 내에서의 위치와 같은 요인에 영향을 받는다. 시료가 필라멘트와 직접 접촉하지 않기 때문에 정확한 열분해 온도 및 시간을 결정하기 어렵다. 불균일한 가열에 의한 열전달의 변화로 인해 온도 정확도와 재현성이 떨어질 수 있다.24-26
3. Curie point pyrolyzer
퀴리점 열분해기(Curie point pyrolyzer)는 금속의 강자성(ferromagnetic) 성질을 이용한 가열 방식으로 고주파 전자기장과의 상호작용에 의해 특정 온도로 빠르게 가열된다.23,25,27 퀴리점(퀴리 온도)는 강자성 물질이 자성을 잃는 정확하고 재현성이 우수한 온도이다.25 퀴리점 온도에 도달하면 강자성 특성이 사라져 더 이상 가열되지 않는다. 퀴리점 열분해기에서 시료는 얇은 강자성 호일(pyrofoil)에 싸여 예열된 회화로에 도입된다.24,26,30 유도 가열에 의해 pyrofoil의 온도가 급격하게 퀴리점까지 상승하고 열이 시료에 전도되어 열분해가 일어난다. 퀴리점 열분해기에서 열분해 온도는 pyrofoil의 종류에 의해 결정된다.23,29,31 퀴리점 열분해기에서 사용하는 pyrofoil은 주로 니켈과 철의 합금이다.31 그 외에 철과 코발트 등으로 제조된 합금을 이용하기도 한다. 시료의 가열은 일반적으로 10-100 ms 사이의 매우 짧은 시간에 일어나며, pyrofoil의 종류에 따라 160-1040 °C까지 약 20개 이상의 열분해 온도 선택이 가능하다.23,28 퀴리점 열분해기는 빠른 가열 속도, 정확한 온도 재현성을 가지고 있으나, 사용하는 pyrofoil의 종류에 따라 열분해 온도가 정해져 있으며 다른 온도 단계를 프로그래밍할 수 없다는 단점이 있다.18,25,32
4. Double-shot pyrolyzer
이중 분석 열분해기(double-shot pyrolyzer)는 휘발성 및 비휘발성 화합물에 대한 정보를 모두 얻을 수 있는 방법이다.25 시료는 스테인리스 스틸 시료 컵에 위치하며 중력에 의해 시료 컵이 마이크로 회화로 중심으로 이동된다.24 회화로의 온도는 미리 설정되어 있으며 시료는 주입 즉시 열분해가 진행된다. 다단계 열분해 작업을 위해 열 탈착 및 열분해가 수반된다. 저분자량의 휘발성 화합물은 저온에서 열 탈착 단계를 거쳐 분석된다.25 이중 분석 열분해기를 이용한 분석은 두 단계로 이루어진다. 첫 번째 단계에서는 휘발성 화합물이 열 탈착 후 GC/MS로 분석되고, 두 번째 단계에서는 남은 비휘발성 유기물인 고분자 등의 시료가 열분해 되어 GC/MS로 분석된다. 온도는 40-800 °C 범위에서 1 °C간격으로 조절 가능하며, 승온 속도는 1-60 °C/min까지 조절할 수 있다.
Microstructural Analysis of SBR Using Pyrolytic Technique
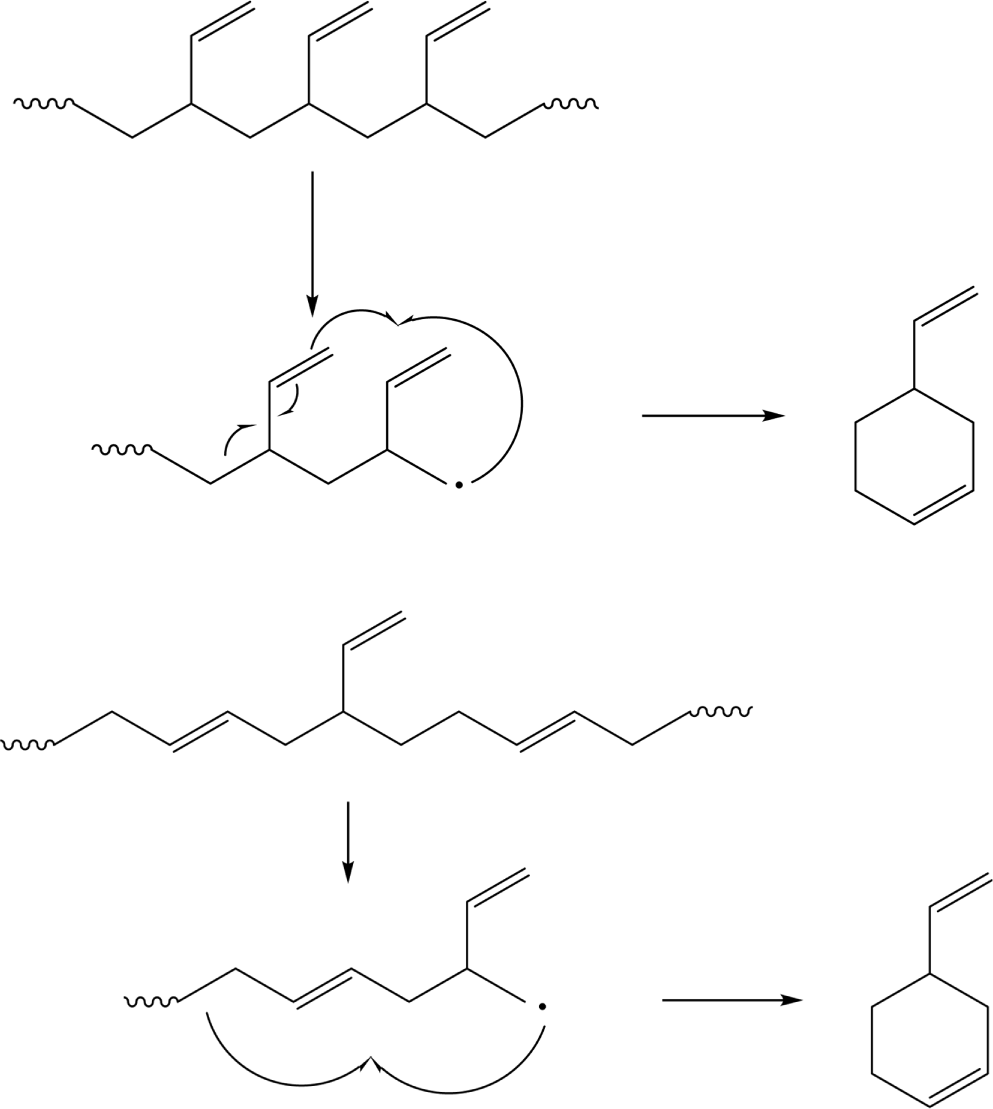
SBR의 열분해생성물은 기본적으로 BR의 열분해 생성물을 포함한다. BR의 주요 열분해 생성물은 butadiene, 4-vinyl-cyclohexene(4-VCH)가 있다.1,3,18,33 이외의 SBR 열분해생성물은 styrene, 2-phenylpropene(2-PP), 3-phenylcyclopentene (3-PCP), 4-phenylcyclohexene(4-PCH) 등이 있다.2-5,18,33 각 열분해생성물의 형성 메커니즘을 Schemes 1-4에 나타냈다. 4-VCH의 경우 1,4-unit이나 1,2-unit의 butadiene sequence에 의해 생성되며, 2-PP의 경우에는 butadiene-styrene hetero-sequence인 1,4-unit-styrene과 1,2-unit-styrene 조합에서 생성된다. 3-PCP과 4-PCH는 1,2-unit-styrene heterosequence에서 형성된다. 4-PCH는 1,4-unit-styrene heterosequence에서도 형성될 수 있다.
Scheme 1.
Pyrolysis mechanism for formation of 4-vinylcyclohexene (4-VCH) from butadiene sequence.
Download Original Figure
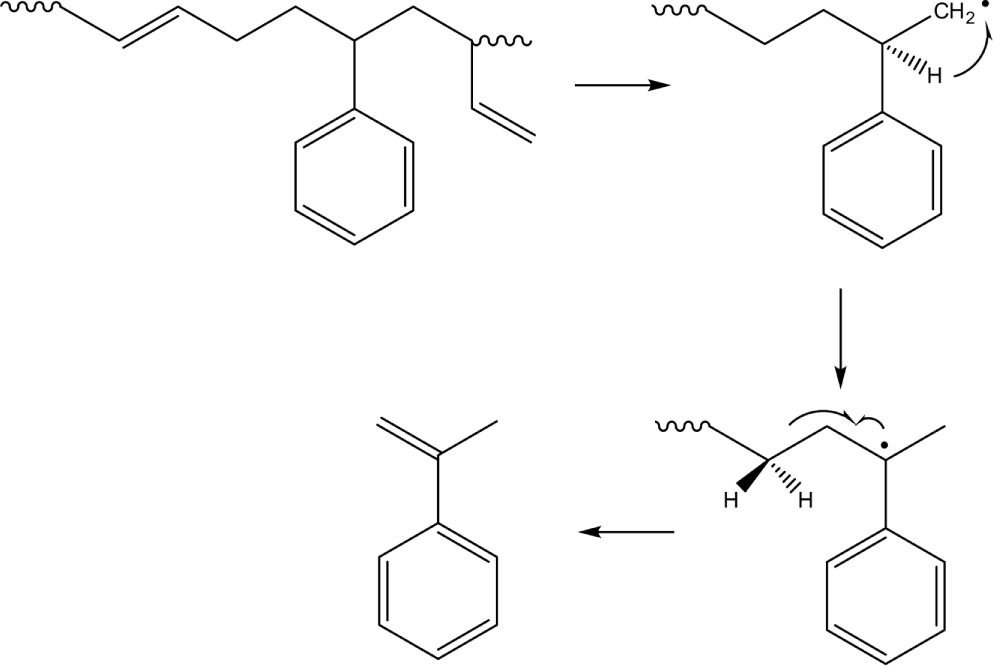
Scheme 2.
Pyrolysis mechanism for formation of 2-phenylpropene (2-PP) from butadiene-styrene heterosequence of SBR.
Download Original Figure
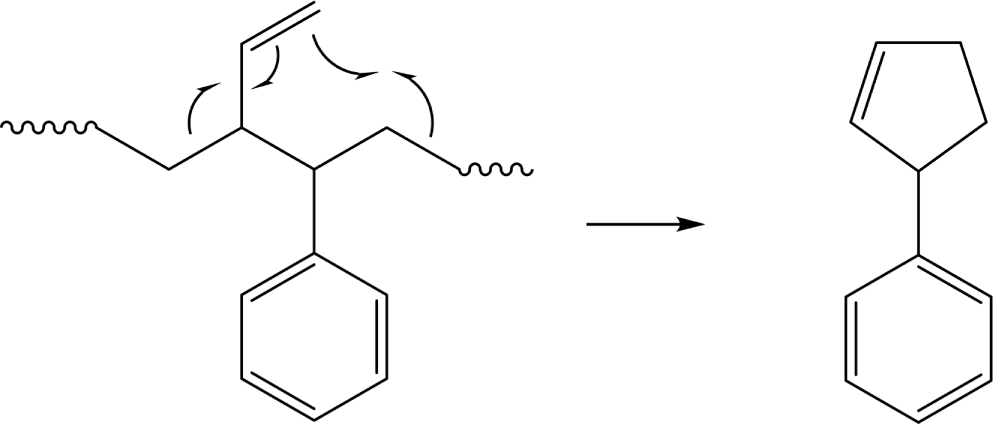
Scheme 3.
Pyrolysis mechanism for formation of 3-phenylcyclopentene (3-PCP) from butadiene-styrene heterosequence of SBR.
Download Original Figure
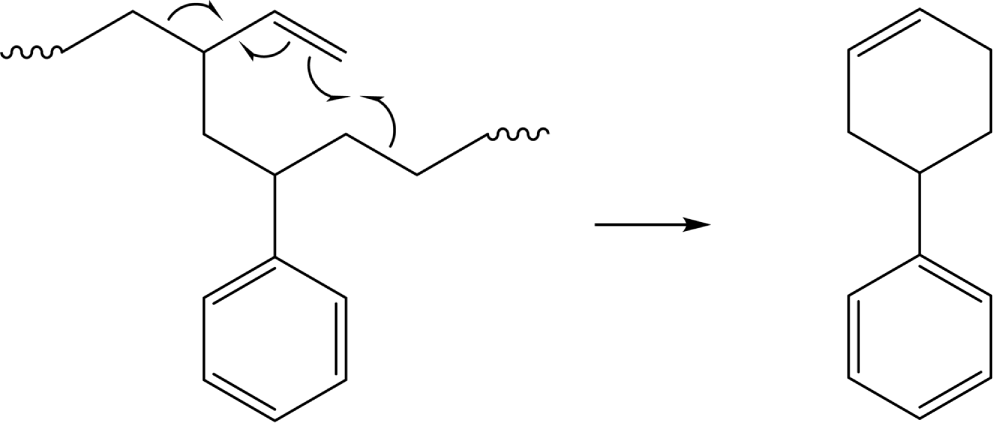
Scheme 4.
Pyrolysis mechanism for formation of 4-phenylcyclohexene (4-PCH) from butadiene-styrene heterosequence of SBR.
Download Original Figure
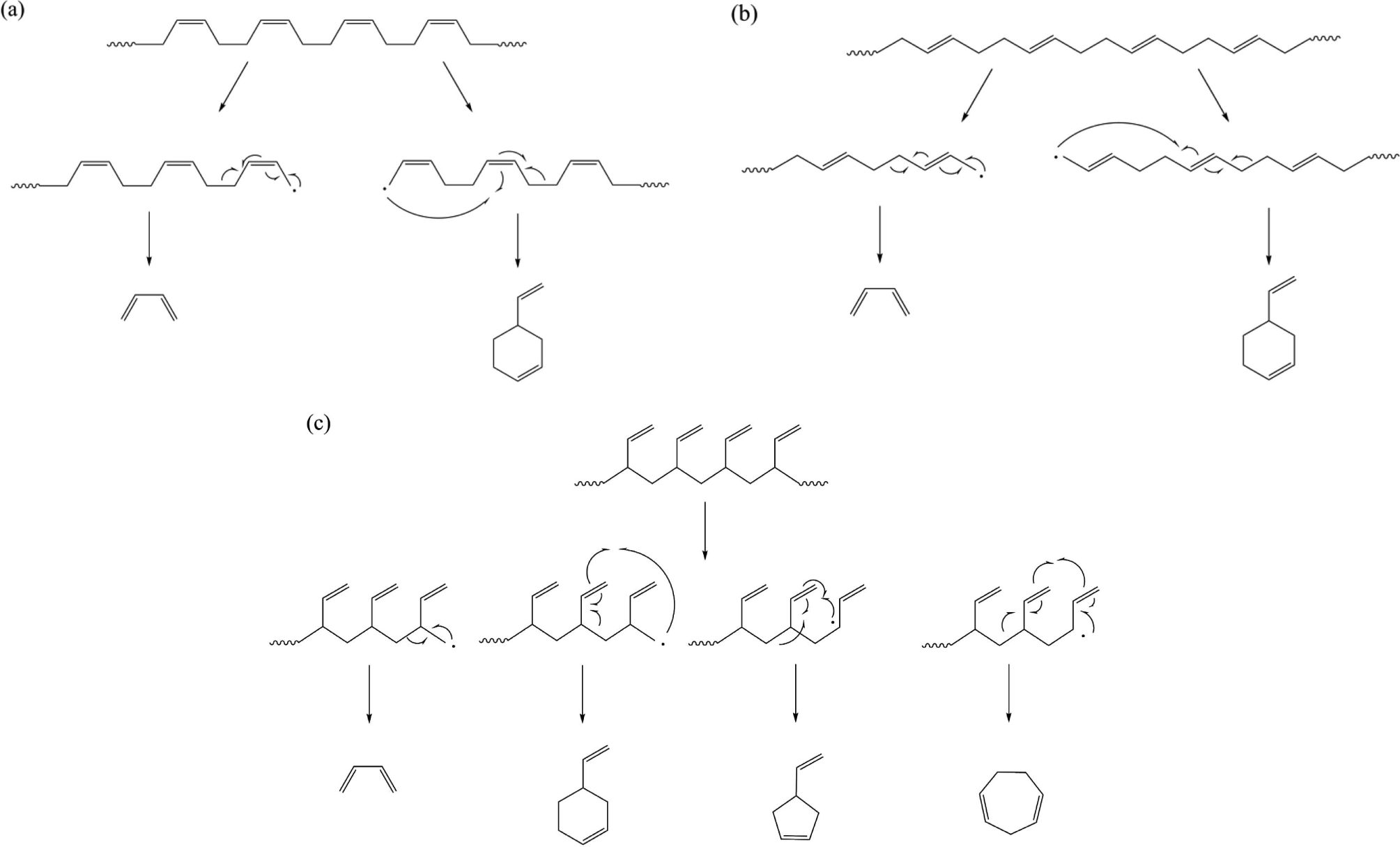
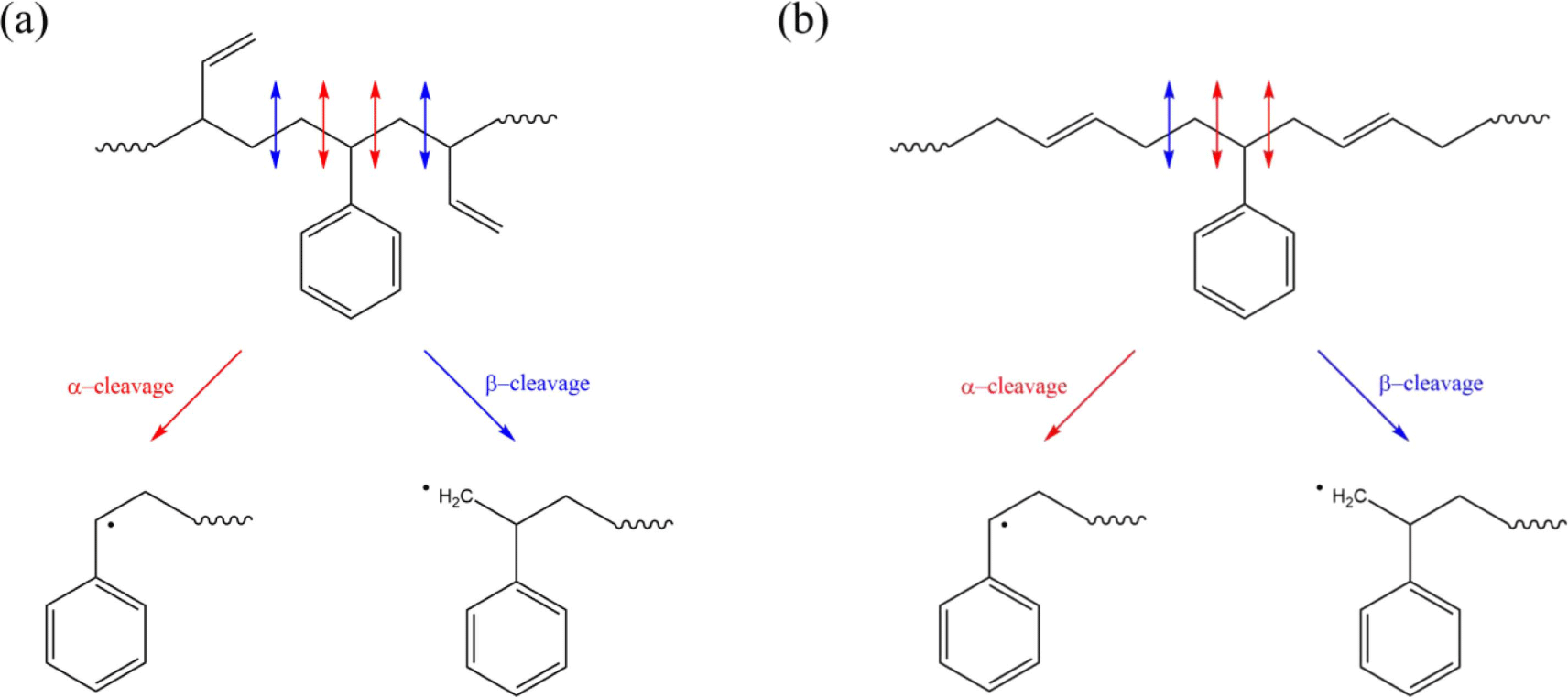
Table 1에 SBR의 미세구조 함량이 증가함에 따라 주요 열분해생성물의 변화 경향을 요약하였다. 1,4-Unit은 1,2-unit에 비하여 butadiene을 생성하는 것이 상대적으로 활발하지 않다.18 이에 반해 1,2-unit은 그 존재에 따라 열분해생성물의 종류에 영향을 미친다.1,3,4,35 1,2-Unit에서는 4-VCH 이외에 4-vinylcyclopentene과 1,4-cycloheptadiene과 같은 C7 종이 생성될 수 있어서, 1,4-unit 대비 상대적으로 4-VCH가 적게 생성된다.3,4,35Scheme 5에서와 같이 C7 종은 2차 라디칼에서 형성된다. 하지만 cis-1,4-unit와 trans-1,4-unit에서는 1차 라디칼만 생성되므로 1,2-unit ho-mosequence에서만 C7 종이 형성될 수 있다. 이에 따라 styrene 함량이 유사할 때, 1,2-unit이 증가함에 따라 C7 종의 열분해생성물이 형성될 수 있으므로 4-VCH의 생성은 감소한다. SBR에서 styrene 함량의 증가는 열분해생성물로 styrene의 생성을 활발하게 한다.3,34,36 1,2-Unit-styrene heterosequence는 2-PP의 생성을 촉진시키는 반면, 1,4-unit-styrene heterosequence에서는 2-PP가 생성되지 않는다.4,5,18 이는 열분해 되면서 형성되는 서로 다른 라디칼에 의한 것이다.1,2Scheme 6에서와 같이 α-cleavage에 의해서는 styrene이 형성되며 β-cleavage에 의해서 2-PP가 생성된다. 1,2-Unit-styrene heterosequence가 1,4-unit-styrene hetero-sequence보다 β-cleavage가 형성될 수 있는 가능성이 높기 때문에 1,2-unit-styrene heterosequence가 증가함에 따라 2-PP도 증가한다.
Table 1.
Variation in Abundances of Pyrolysis Products with Microstructure of SBR
| Microstructure of SBR |
Increase |
Decrease |
Reference |
| Styrene |
Styrene |
– |
3 |
| 1,4-Unit |
4-Vinylcyclohexene |
– |
3,4 |
| 1,2-Unit |
– |
4-Vinylcyclohexene |
3,4 |
| 1,4-Unit-Styrene |
– |
2-Phenylpropene |
5,18 |
| 1,2-Unit-Styrene |
2-Phenylpropene |
– |
4,5,18 |
Download Excel Table
Scheme 5.
Principal pyrolysis products formed from (a) cis-1,4-unit, (b) trans-1,4-unit, and (c) 1,2-unit butadiene sequences.
Download Original Figure
Scheme 6.
Primary radical formation from (a) 1,2-unit-styrene and (b) 1,4-unit-styrene heterosequences by heating.
Download Original Figure
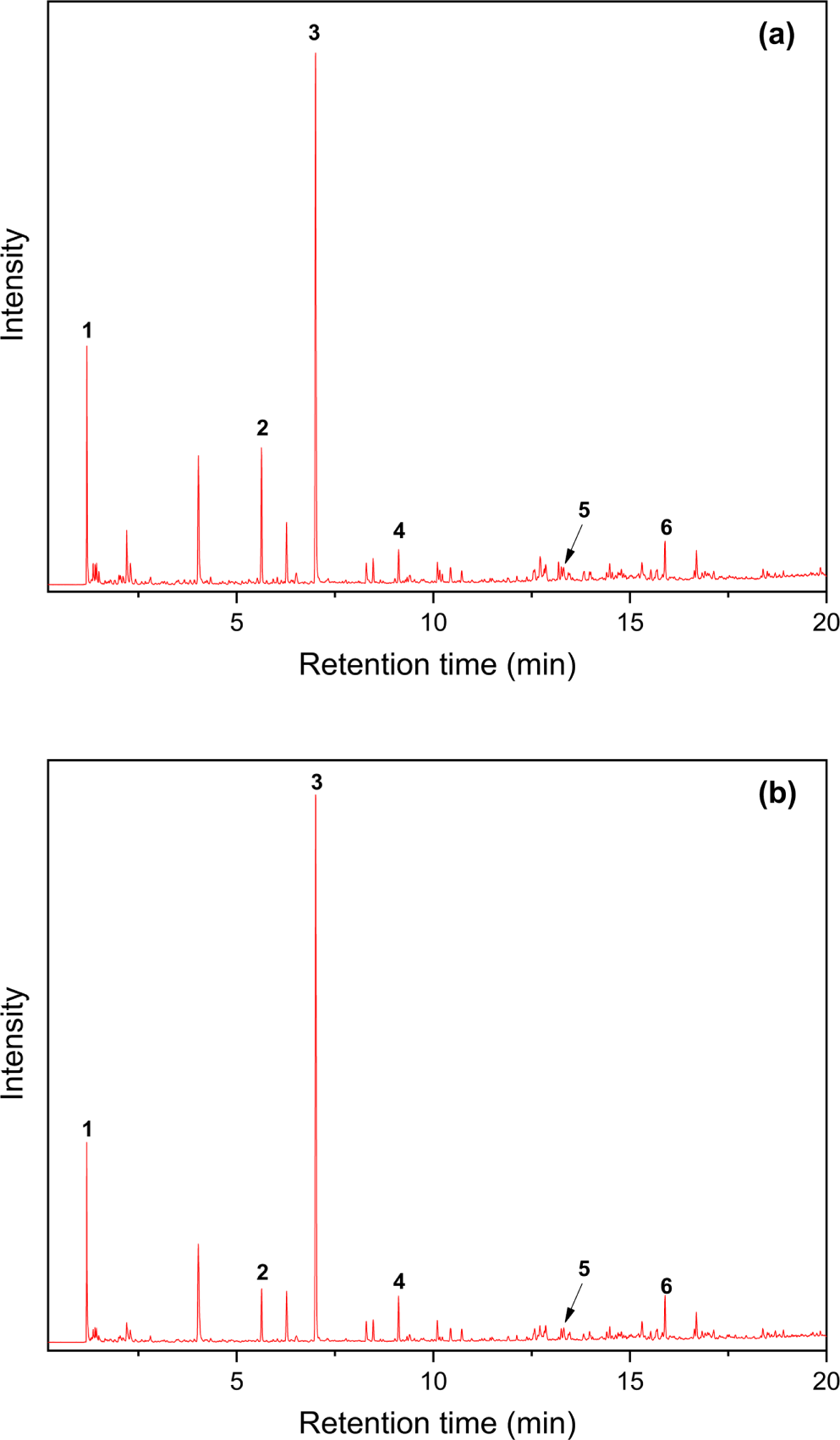
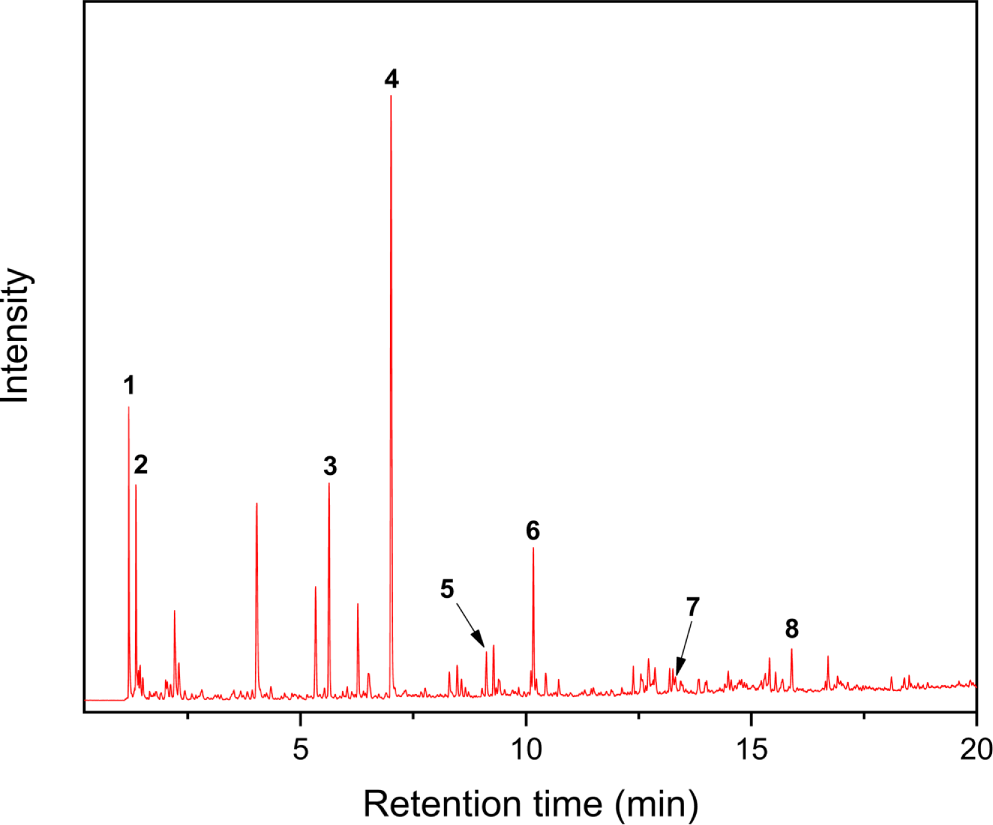
Figure 1과 Table 2에는 ESBR과 SSBR의 전형적인 Py-GC/MS 크로마토그램을 실었다. 여기서 눈여겨볼 점은 1,2-unit의 함량이 더 높은 SSBR에서 styrene 대비 4-VCH의 비율이 더 작게 나타난다는 것이다. 이는 위에서 언급했듯이 1,2-unit이 더 높은 함량일 때에는 4-VCH 이외에 C7 종의 열분해 생성물이 형성될 수 있기 때문이다.
Figure 1.
Py-GC/MS chromatograms of (a) ESBR and (b) SSBR (styrene: 40.1 wt%, 1,2-unit: 46.6 mol%, 1,4-unit: 53.6 mol%).
Download Original Figure
Table 2.
Principal Pyrolysis Product Formed from ESBR and SSBR (Figure 1)
| Peak No. |
Retention time (min) |
Pyrolysis products |
| 1 |
1.18 |
Butadiene |
| 2 |
5.63 |
4-Vinylcyclohexene |
| 3 |
7.01 |
Styrene |
| 4 |
9.12 |
2-Phenylpropene |
| 5 |
13.32 |
3-Phenylcyclopentene |
| 6 |
15.89 |
4-Phenylcyclohexene |
Download Excel Table
SBR의 미세구조는 열분해생성물과 밀접한 관계가 있다.18 SBR의 열분해생성물 중 2-PP의 상대비는 1,2-unit 함량이 증가할수록 증가하는 경향을 보였으며, 1,4-unit 함량이 증가하면 감소하는 경향을 보였다. 또한 다른 열분해생성물에 비하여 그 상관성이 높은 것으로 나타났다. 이와 같은 상관관계를 이용하면 가교된 미지의 SBR 시료에서 1,2-unit과 1,4-unit의 함량을 분석할 수 있다. 미지 원재료 SBR 시료에서 butadiene과 styrene의 함량의 분석을 위하여 styrene에 대한 butadiene의 상대비와 전체 butadiene의 함량을 비교하였으나, 상관계수가 0.663으로 상당히 낮게 나타났다. 상관성을 높이기 위해 1,2-unit 함량을 곱하여 보정하면 상관계수는 0.943으로 개선되어 미지 시료의 미세구조 결정에 이용할 수 있다. 가황 SBR에서는 열분해생성물로 butadiene이 1,2-unit 함량과 전체 butadiene 함량에 따라 증가하는 경향을 보이며 높은 상관계수를 나타내므로, 가황 SBR의 1,2-unit 혹은 전체 butadiene 함량을 결정할 수 있음을 의미한다.
원재료와 가황물은 미세구조에 따라 열분해생성물이 다른 경향이 나타내었다.5,18 1,2-Unit이 증가함에 따라 2-PP의 상대비가 증가하는 경향은 원재료에서 잘 나타났으나 가황물에서는 상관계수가 낮았다. 그 이유는 가교, cis/trans conversion 등에 의한 것으로 보인다. 충진제와 실란커플링제도 SBR의 열분해생성물의 형성에 영향을 미친다.2 Butadiene/styrene 비율은 실란커플링제 함량과 관계없이 거의 유사한 값을 가졌다. 하지만 1,4-cycloheptadiene/VCH의 비는 실란커플링제 함량이 증가함에 따라 증가하였으며, 배합물에서보다 가황물에서 더 크게 나타났다. 가교에 의해 형성된 C-S 결합은 고무 주쇄의 C-C결합보다 약해서 보다 쉽게 끊어지므로 열분해생성물의 형성에 영향을 준다.
Quantification of SBR in SBR-Blended Rubber Composites Using Pyrolytic Technique
1. Analysis of SBR/NR binary blend
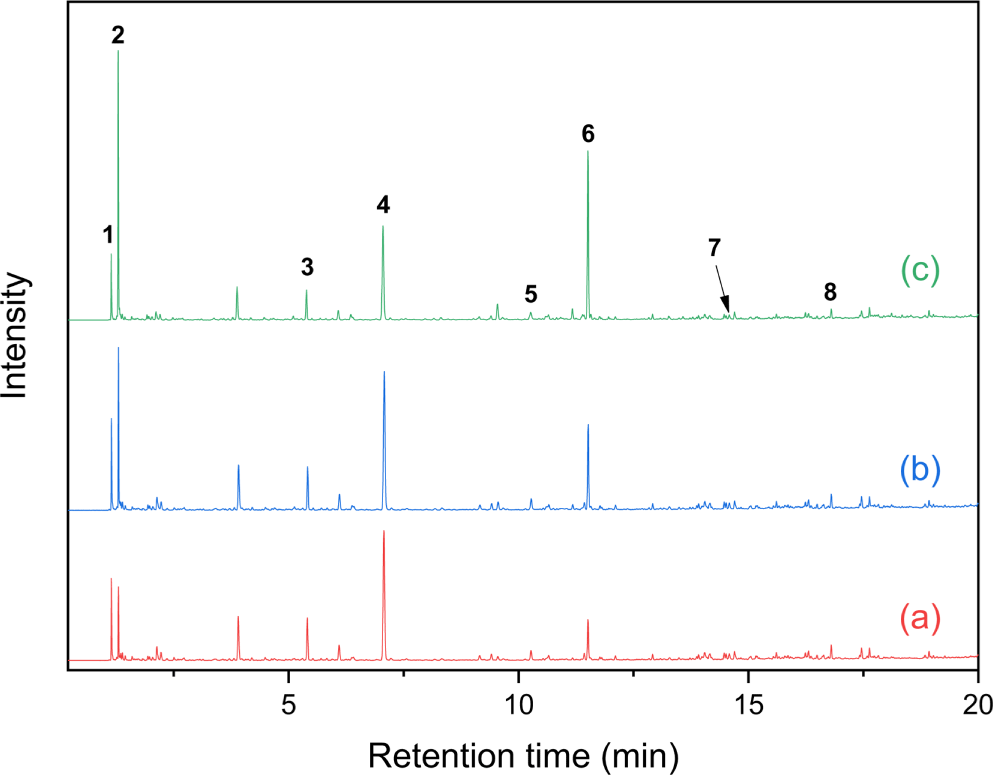
Figure 2는 원재료 ESBR과 NR을 ESBR/NR = 90/10, 80/20, 60/40의 무게비로 혼합하여 얻은 Py-GC/MS 크로마토그램이다. Table 3에 검출된 주요 열분해생성물을 정리하였다. Isoprene과 limonene(dipentene)은 NR의 주요 열분해 생성물이다. SBR의 비율이 증가함에 따라 SBR의 열분해생성물은 증가하였으며, NR의 열분해생성물은 감소하였다. SBR과 NR의 특징적인 열분해 생성물로써 주로 styrene과 limonene을 선택한다. ESBR과 NR의 비율에 따른 styrene/limonene의 봉우리 면적비를 비교했을 때 ESBR의 함량이 10, 20, 40%로 증가함에 따라 styrene/limonene의 봉우리 면적비는 0.80, 2.27, 5.01로 증가하였다.
Table 3.
Principal Pyrolysis Product Formed from ESBR/NR Blend (Figure 2)
| Peak No. |
Retention time (min) |
Products |
| 1 |
1.14 |
Butadiene |
| 2 |
1.30 |
Isoprene |
| 3 |
5.41 |
4-Vinylcyclohexene |
| 4 |
7.07 |
Styrene |
| 5 |
10.27 |
2-Phenylpropene |
| 6 |
11.51 |
Limonene |
| 7 |
14.58 |
3-Phenylcyclopentene |
| 8 |
16.80 |
4-Phenylcyclohexene |
Download Excel Table
일반적으로 SBR과 NR이 혼합된 고무에서 두 성분의 조성비를 분석할 때 주요 열분해생성물로 styrene과 limonene을 사용한다.37-41 두 열분해생성물의 봉우리 면적 혹은 특정 이온의 봉우리 면적을 이용하여 고무 조성을 예측할 수 있다. Styrene의 봉우리 면적을 Asty, limonene의 봉우리 면적을 Alim이라고 했을 때, 다음 식을 이용하여 SBR/NR 혼합에서 SBR의 분율(FSBR)을 계산한다.
SBR과 NR의 혼합 비율이 다른 시료를 준비하여 열분해 분석한 결과를 사용하여 SBR의 비율에 따른 FSBR을 도식화하여 검량선을 작성하고, 미지 시료의 결과를 대입하여 고무 조성을 결정한다.
Yang 등은 카본블랙이 포함되지 않은 고무를 표준물질로 하여 검량선을 작성하였으며, 이를 카본블랙으로 충진한 고무를 분석하여 입증하였다.38 Yang 등의 연구 결과는 다음과 같다. 충진하지 않은 SBR/NR 고무의 블렌드 비율을 0-90% 사이에서 10% 간격으로 변화시켜 시료를 준비하였다. 검량선 작성은 표준 고무를 용액으로 제조하였다. 가교된 시험고무는 0.02 g을 이용하여 가교구조를 끊기 위해 10 mL 과산화수소에 넣고 끓인 후 4시간동안 전기로에서 가열하였다. 그 후 10 mL의 사이클로헥산을 이용하여 고무를 추출하였다. 이 용액을 50 °C에서 72시간 동안 방치하였다. 고무 용액 50 μL를 분석에 이용하였으며, 용매를 증발시켜 고무만을 열분해하였다. 열분해는 GC/MS에 직접 부착된 수직 마이크로 전기로 열분해기(vertical microfurnace pyrolyzer)를 사용하여 수행하였다. 열분해는 550 °C에서 진행되었다. SBR과 NR의 특징적인 열분해 생성물로 styrene과 limonene을 사용하였다. 검량선은 우수한 상관성(상관계수 R2 = 0.999)을 나타냈다. SBR/NR = 50/50의 시험고무를 분석하여 검량선을 통해 고무 비율을 계산하였을 때 SBR의 비율이 48.5%로 거의 유사한 값을 얻을 수 있었다.
2. Analysis of SBR/BR binary blend
Figure 3과 Table 4에 ESBR과 BR의 혼합비를 다르게 하여 얻은 Py-GC/MS 크로마토그램과 주요 열분해생성물을 제시하였다. SBR과 BR은 주요 열분해생성물 중 일부가 동일하게 나타난다. BR에서 생성되는 열분해생성물은 SBR의 butadiene sequence에서 동일하게 생성된다. SBR의 함량이 감소함에 따라 butadiene과 4-VCH는 일부 증가하며, 2-PP, 3-PCP, 4-PCH는 감소하는 경향을 보였다. Butadiene과 4-VCH는 SBR과 BR의 공통적인 열분해생성물이므로 BR이 증가함에 따라 증가하는 경향을 보인다. 따라서 SBR과 BR의 혼합고무에서 조성을 분석하기 위해서는 butadiene-styrene의 heterosequence에서 형성되는 열분해 생성물에 의한 보정이 필요하다.
Table 4.
Principal Pyrolysis Product Formed from ESBR/BR Blend (Figure 3)
| Peak No. |
Retention time (min) |
Products |
| 1 |
1.18 |
Butadiene |
| 2 |
5.63 |
4-Vinylcyclohexene |
| 3 |
7.01 |
Styrene |
| 4 |
9.12 |
2-Phenylpropene |
| 5 |
13.32 |
3-Phenylcyclopentene |
| 6 |
15.89 |
4-Phenylcyclohexene |
Download Excel Table
SBR과 BR이 혼합된 고무에서 조성을 분석할 때 지표 열분해생성물로 styrene과 4-VCH를 일반적으로 사용한다.37,38,40 SBR/NR의 혼합고무를 분석하는 방식과 마찬가지로 지표 열분해생성물의 봉우리 면적을 이용하여 고무 조성을 결정한다. Styrene의 봉우리 면적을 Asty, 4-VCH의 봉우리 면적을 AVCH이라고 했을 때, 다음 식을 이용하여 SBR/NR 혼합에서 SBR의 분율(FSBR)을 계산한다.
SBR과 BR의 혼합 비율이 다른 시료를 준비하여 열분해 분석한 결과를 사용하여, SBR의 비율에 따른 FSBR을 도식화하여 검량선을 작성하고, 미지 시료의 결과를 여기에 대입하여 고무 조성을 결정한다.
Yang 등은 충진되지 않은 SBR/BR 혼합물로 검량선을 작성하고 카본블랙이 포함된 고무로 검량선을 평가하였다.38 그 결과, 검량선의 상관계수가 R2 = 0.987로 우수하였으며, 카본블랙으로 충진된 SBR/BR = 50/50 시료를 분석한 결과 SBR의 비율이 51.6%인 것으로 나타났다. Lee 등도 유사한 실험을 진행한 결과, 상관계수(R2 = 0.980)가 우수한 검량선을 얻었다고 보고하였다.37
Chae와 Choi는 SBR/BR 혼합 고무 성분비를 분석하기 위해 원재료 고무 용액을 이용하여 검량선을 작성하였다.42 가황 고무의 성분비를 분석하기 위하여 가황물 시험편을 제조하여 표준시료를 사용하는 것이 마땅하지만, 시간과 비용이 요구되며 미지시료의 배합사양을 알 수 없다는 어려움이 따르기 때문에 원재료를 이용한 검량선 분석을 통해 가황물을 대신할 수 있는 지표를 제안하였다. SBR/BR 혼합 고무 제조를 위하여 2가지 방법을 사용하였다. 하나는 혼합 고무 용액을 제조하였으며 다른 하나는 각 용액을 시료 준비 과정에서 혼합하여 사용하였다. 각 시료는 슬라이드 글라스에 캐스팅하여 용매를 완전 건조시킨 후, 구 형태로 제조하여 분석하였다. 원재료를 이용하여 작성한 검량선을 가황물 시료를 사용하여 작성한 검량선과 비교한 결과, 원재료와 가황물의 검량선이 유사한 기울기를 갖는 지표는 butadiene/styrene과 2-PP/butadiene이었다.
3. Analysis of SBR/NR/BR ternary blend
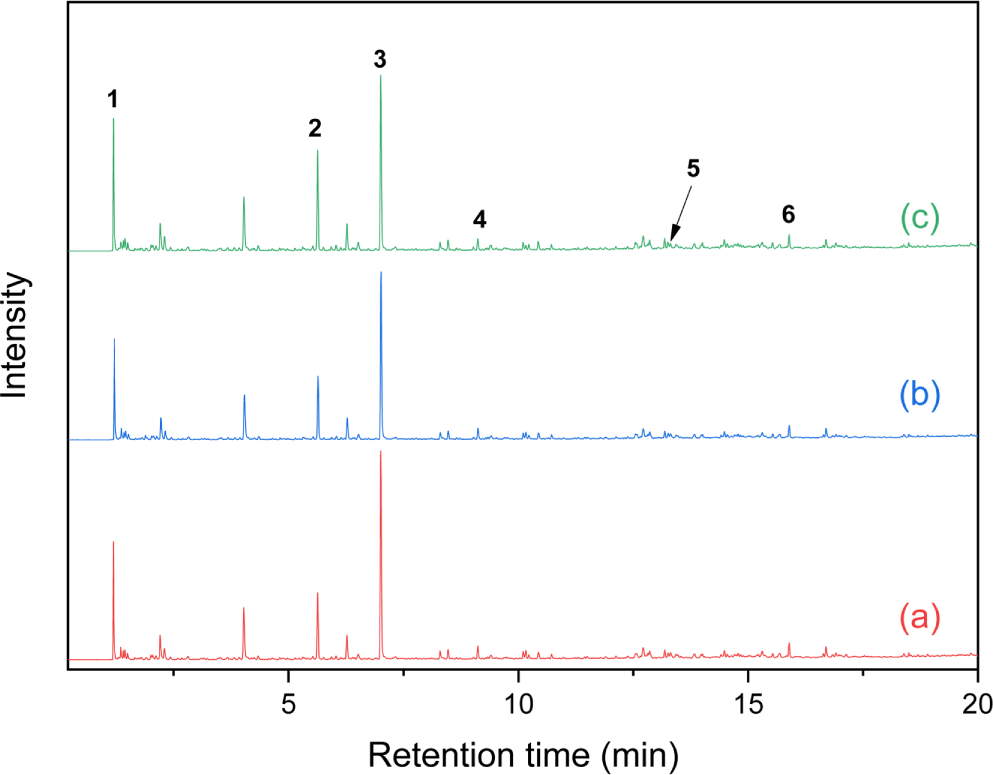
Figure 4와 Table 5에 ESBR/NR/BR의 3성분계 혼합 고무의 Py-GC/MS 크로마토그램과 주요 열분해생성물을 제시하였다. SBR과 BR의 주요 열분해생성물인 butadiene과 4-VCH가 검출되었으며, SBR의 특징적인 열분해생성물인 2-PP, 3-PCP, 4-PCH도 검출되었다. NR의 주요 열분해 생성물인 isoprene과 limonene도 검출되었다.
Table 5.
Principal Pyrolysis Product Formed from ESBR/NR/BR Blend (Figure 4)
| Peak No. |
Retention time (min) |
Products |
| 1 |
1.19 |
Butadiene |
| 2 |
1.35 |
Isoprene |
| 3 |
5.63 |
4-Vinylcyclohexene |
| 4 |
7.01 |
Styrene |
| 5 |
9.12 |
2-Phenylpropene |
| 6 |
10.17 |
Limonene |
| 7 |
13.32 |
3-Phenylcyclopentene |
| 8 |
15.89 |
4-Phenylcyclohexene |
Download Excel Table
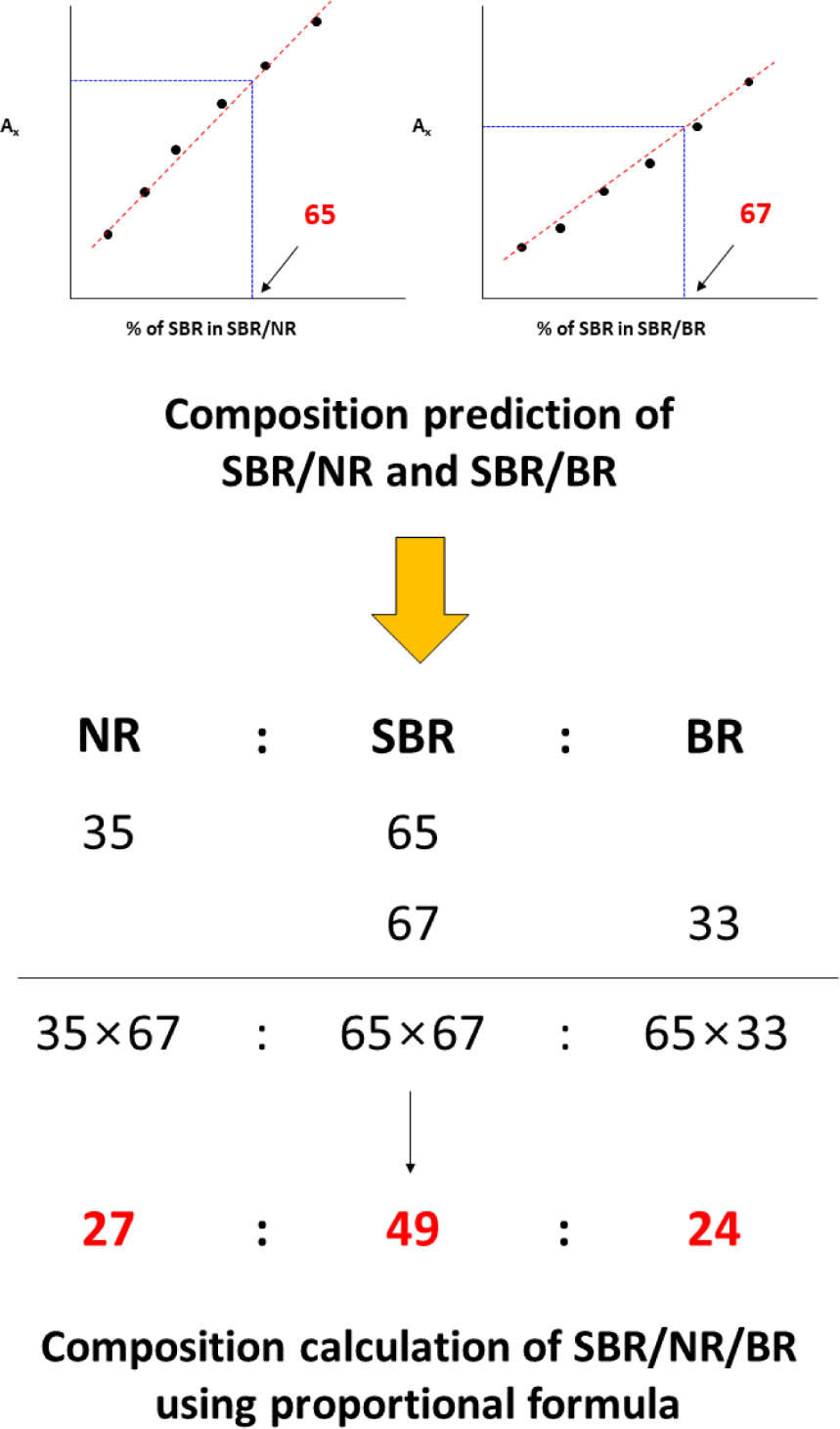
Lee 등과 Huh 등은 SBR/NR, SBR/BR의 이원 블렌드 고무의 정량분석결과를 이용하여 SBR/NR/BR의 조성 비율을 결정하고자 하였다.37,40 NR, SBR, BR의 특징적인 열분해 생성물인 limonene, styrene, 4-VCH를 사용하여 이원 블렌드 고무의 검량선을 작성하였다. 이원 블렌드 고무 분석을 통해 얻은 SBR/NR과 SBR/BR 예측 값을 비례 계산식을 이용하여 SBR/NR/BR의 조성을 계산하였다. 이 과정은 Figure 5에 나타내었다. 예를 들어 SBR/NR/BR = 50/25/25인 시료를 분석하여 얻은 SBR/NR과 SBR/BR의 조성이 65/35와 67/33일 때, 비례 관계식을 통해 SBR/NR/BR = 49/27/24로 계산할 수 있다. 실제 값과 거의 유사한 조성을 얻을 수 있었다.
Acknowledgements
이 연구는 2020년도 산업통상자원부 및 산업기술평가관리원(KEIT) 연구비 지원에 의한 연구임(과제번호 20010851).
References
S.-S. Choi and H.-M. Kwon, “Analytical method for determination of butadiene and styrene contents of styrene-butadiene rubber vulcanizates without pretreatment using pyrolysis-gas chromatography/mass spectrometry”,
Polym. Test,
38, 87 (2014).


S.-S. Choi, “Influence of silane coupling agent on pyrolysis pattern of styrene-butadiene rubber in filled rubber compounds”,
Bull. Korean Chem. Soc.,
22, 1145 (2001).

S.-S. Choi, “Characteristics of the pyrolysis patterns of styrene-butadiene rubbers with differing microstructure”,
J. Anal. Appl. Pyrolysis,
62, 319 (2002).


S.-S. Choi and H.-M. Kwon, “Characterization of pyrolysis products formed from styrene-1,2-unit heterosequence of styrene-butadiene copolymer”,
J. Anal. Appl. Pyrolysis,
99, 1 (2013).


S.-S. Choi and H.-M. Kwon, “Analytical method for determination of microstructures of solution styrene-butadiene copolymers using 2-phenylpropene/styrene ratio of pyrolysis products”,
Polym. Test,
44, 153 (2015).


S.-S. Choi, Y. Kim, and H.-M. Kwon, “Microstructural analysis and cistrans isomerization of BR and SBR vulcanizates reinforced with silica and carbon black using NMR and IR”,
RSC Adv.,
4, 31113 (2014).


S.-S. Choi, Y. Kim, and H.-M. Kwon, “Analytical considerations for determination of the microstructures of sulfur-cured solution styrene-butadiene rubbers”,
Polym. Int.,
66, 803 (2017).


N. J. Morrison and M. Porter, “Temperature effects on the stability of intermediates and crosslinks in sulfur vulcanization”,
Rubber Chem. Technol.,
57, 63 (1984).


S.-S. Choi and G. Cho, “Influence of 1,2-unit contents on retraction behaviors of SBR vulcanizates”,
J. Appl. Polym. Sci.,
102, 4707 (2006).


S.-S. Choi and J.-C. Kim, “Thermal aging behaviors of weather resistant rubber composites of EPDM, IIR, and BIIR”,
Elast. Comp.,
47, 148 (2012).


S.-S. Choi and J.-C. Kim, “Influence of the 1,2-unit content of SBR and filler systems on thermal aging behaviors of SBR composites”,
J. Ind. Eng. Chem,
13, 950 (2007).

Y. Kim and S.-S. Choi, “Microstructural analysis of SBR blends using infrared spectroscopy”,
Elast. Comp.,
49, 103 (2014).


X. Liu, S. Zhao, X. Zhang, X. Li, and Y. Bai, “Preparation, structure, and properties of solution-polymerized styrene-butadiene rubber with functionalized end-groups and its silica-filled composites”,
Polymer,
55, 1964 (2014).


J. Zhang, H. Chen, Y. Zhou, C. Ke, and H. Lu, “Compatibility of waste rubber powder/polystyrene blends by the addition of styrene grafted styrene butadiene rubber copolymer: effect on morphology and properties”,
Polym. Bull.,
70, 2829 (2013).


C. B. B. Luna, E. M. Araújo, D. D. Siqueira, D. D. S. Morais, E. A. S. Filho, and M. V. L. Fook, “Incorporation of a recycled rubber compound from the shoe industry in polystyrene: effect of SBS compatibilizer content”,
J. Elastomers Plast.,
52, 3 (2019).


K.-H. Kim, J.-Y. Lee, J.-M. Choi, H.-J. Kim, B. Seo, B.-S. Kim, G.-H. Kwag, H.-J. Paik, and W. Kim, “Synthesis of ionic elastomers based on styrene-butadiene rubber containing methacrylic acid”,
Elast. Compos.,
48, 46 (2013).


S. Khoee and M. Sorkhi, “Microstructure analysis of brominated styrene-butadiene rubber”,
Polym. Eng. Sci.,
47, 87 (2007).


권혁민, “SBR 열분해 생성물의 특성 연구”, 세종대학교 석사학위논문, 2014.

S. R. Shield, G. N. Ghebremeskel, and C. Hendrix, “Pyrolysis-GC/MS and TGA as tools for characterizing blends of SBR and NBR”,
Rubber Chem. Technol.,
74, 803 (2001).


R. P. Lattimer, K. M. Schur, W. Windig, and H. L. C. Meuzelaar, “Quantitative analysis of rubber triblends by pyrolysis-mass spectrometry”,
J. Anal. Appl. Pyrolysis,
8, 95 (1985).


E. Grieco, M. Bernardi, and G. Baldi, “Styrene-butadiene rubber pyrolysis: products, kinetics, modelling”,
J. Anal. Appl. Pyrolysis,
82, 304 (2008).


S.-S. Choi and H.-M. Kwon, “Considering factors on determination of microstructures of SBR vulcanizates using pyrolytic analysis”,
Polym. Test.,
89, 106572 (2020).


S. C. Moldoveanu, “Analytical pyrolysis of natural organic polymers”, 1st ed., p.26, Elsevier, Amsterdam, 1998.

C. Watanabe, K. Sato, A. Hosaka, H. Ohtani, and S. Tsuge, “Development of a multifunctional pyrolyzer for evolved gas analysis, thermal desorption, and/or pyrolysis-GC of polymeric materials”,
Am. Lab.,
33, 14 (2001).

Y. Picó and D. Barceló, “Pyrolysis gas chromatography-mass spectrometry in environmental analysis: focus on organic matter and microplastics”,
Trends Anal. Chem.,
130, 115964 (2020).


K. L. Sobeih, M. Baron, and J. Gonzalez-Rodriguez, “Recent trends and developments in pyrolysis-gas chromatography”,
J. Chromatogr. A,
1186, 51 (2008).



A. Lourenco, “The influence of heartwood on kraft delignification of
Eucalyptus globulus wood”, PhD Thesis, Universidade Tecnica de Lisboa, 2012.

N. W. Bower and C. J. K. Blanchet, “Analytical pyrolysis-chromatography: something old, something new”,
J. Chem. Educ.,
87, 467 (2010).


M. R. Grimbley, R. S. Lehrle, R. J. Williams, and D. M. Bate, “An enclosed Curie point pyrolysis-GC technique for studying the oxidative or thermal degradation of polymers and volatile oligomeric oils”,
Polym. Degrad. Stab.,
48, 143 (1995).


C. Pérès, C. Viallon, and J.-L. Berdagué, “Curie point pyrolysis-mass spectrometry applied to rapid characterization of cheeses”,
J. Anal. Appl. Pyrolysis,
65, 161 (2002).


K. Kuroda and D. R. Dimmel, “Effect of pyrofoil composition on pyrolysis of lignin”,
J. Anal. Appl. Pyrolysis,
62, 259 (2002).


S. Buco, M. Moragues, P. Doumenq, A. Noor, and G. Mille, “Analysis of polycyclic aromatic hydrocarbons in contaminated soil by Curie point pyrolysis coupled to gas chromatography-mass spectrometry, an alternative to conventional methods”,
J. Chromatogr. A,
1026, 223 (2004).



T. S. Radhakrishnan and M. Ramarao, “Thermal decomposition of polybutadienes by pyrolysis gas chromatography”,
J. Polym. Sci. Polym. Chem. Ed.,
19, 3197 (1981).


J. Hacaloglu, T. Ersen, N. Ertugrul, M. M. Fares, and S. Suzer, “Pyrolysis mass spectrometric analysis of styrene-butadiene block and random copolymers”,
Eur. Polym. J.,
33, 199 (1997).


S.-S. Choi, “Characteristics of pyrolysis patterns of polybutadienes with different microstructures”,
J. Anal. Appl. Pyrolysis,
57, 249 (2001).


M. Guaita, “Thermal degradation of polystyrene”,
Br. Polym. J.,
18, 226 (1986).


Y. S. Lee, W.-K. Lee, S.-G. Cho, I. Kim, and C.-S. Ha, “Quantitative analysis of unknown compositions in ternary polymer blends: a model study on NR/SBR/BR system”,
J. Anal. Appl. Pyrolysis,
78, 85 (2007).


Z. Yang, G. Fan, Y. Ma, C. Gong, and H. Xu, “A novel quantitative method for analyzing binary rubber blends with characteristics ion by pyrolysis/GC/MS”,
Am. Lab.,
40, 24 (2008).

G. R. Cotten and L. J. Murphy, “Mixing of carbon black with rubber. Ⅵ. Analysis of NR/SBR blends”,
Rubber Chem. Technol.,
61, 609 (1988).


D. S. Huh, J. S. Kim, K. J. Kim, B. K. Ahn, S. K. Suh, and O. K. Han, “Study on analysis of vulcanized rubber by pyrolysis-gas chromatography (Ⅰ) (vulcanizates of NR, BR, and SBR)”,
J. Korea Ins. Rubber Ind.,
22, 11 (1987).

A. Krishen and R. G. Tucker, “Quantitative determination of the polymeric constituents in compounded cured stocks by Curie-point pyrolysis-gas chromatography”,
Anal. Chem.,
46, 29 (1974).


E. Chae and S.-S. Choi, “Building calibration curve for Py-GC/MS analysis of SBR/BR blend rubber compounds”,
Elast. Compos.,
55, 281 (2020).