Introduction
현재 폴리우레탄 산업은 화석연료 사용으로 인한 이산화탄소 배출, 에너지 자원 고갈과 같은 문제점이 제기되어 바이오 기반 폴리우레탄 합성 기술 개발이 활발히 진행되고 있다. 바이오 기반 폴리우레탄은 원재료로 바이오매스인 식물 자원을 사용함으로써, 지구온난화의 주범인 이산화탄소 발생량을 줄일 수 있는 화학소재이다. 식물 자원은 광합성을 위해 이산화탄소를 소모하므로 바이오매스 유래 화학소재를 사용함으로써 잉여 이산화탄소 발생량을 최소화할 수 있다. 바이오매스는 크게 식물성 천연 유지, 목질 계, 해조류로 분류된다.
그 중 식물성 천연 유지는 글리세롤 1분자에 3개의 지방산이 결합된 트리글리세라이드로 이루어져 있다.1 트리글리세라이드를 구성하는 대표적인 지방산으로는 oleic acid, linoleic acid, linolenic acid, ricinoleic acid, stearic acid, palmitic acid 등이 있다.
지방산들 중 ricinoleic acid는 유일하게 하이드록시기(-OH)를 포함하고 있다.2 식물성 유지 중 피마자유는 주로 ricinoleic acid로 이루어져 있고,3 하이드록시기의 존재로 인해 이소시아네이트와 반응하여 폴리우레탄을 형성할 수 있다.4 Ricinoleic acid를 포함하고 있지 않은 대부분의 천연 유지는 하이드록시기를 첨가해주어야 하는데,5 그 방법에는 epoxidation,6 hydro-formylation,7 ozonolysis8가 있다. Ozonolysis(오존 분해)를 통한 방법은 오존(O3)을 이용하여 탄소이중결합을 절단한 후 수소 첨가를 통해 하이드록시기를 도입한다.
Epoxidation(에폭시화) 방법을 통해 합성한 폴리올과 본래 하이드록시기를 가지고 있는 피마자유는 2차 알코올로 이루어져 있으므로 이소시아네이트와의 반응성이 좋은 1차 알코올로 개질 시킬 필요가 있다. 이러한 개질 방법에 alkoxylation9과 transesterification10,11이 있다.
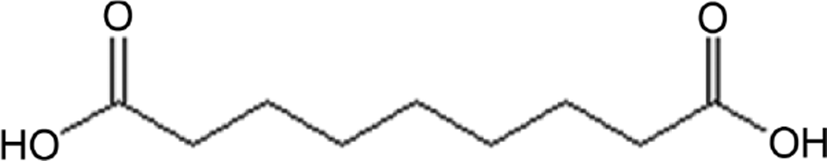
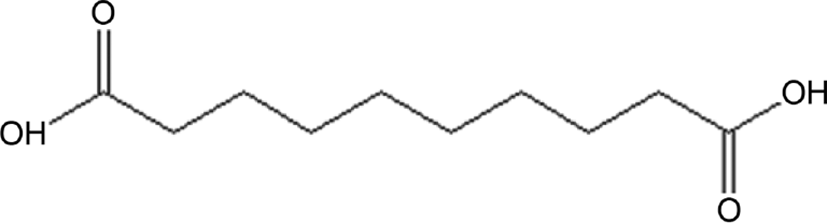
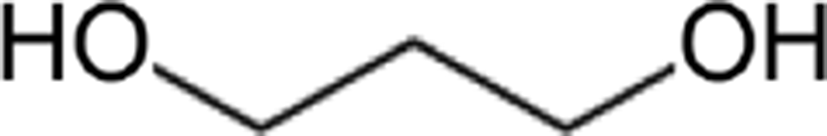
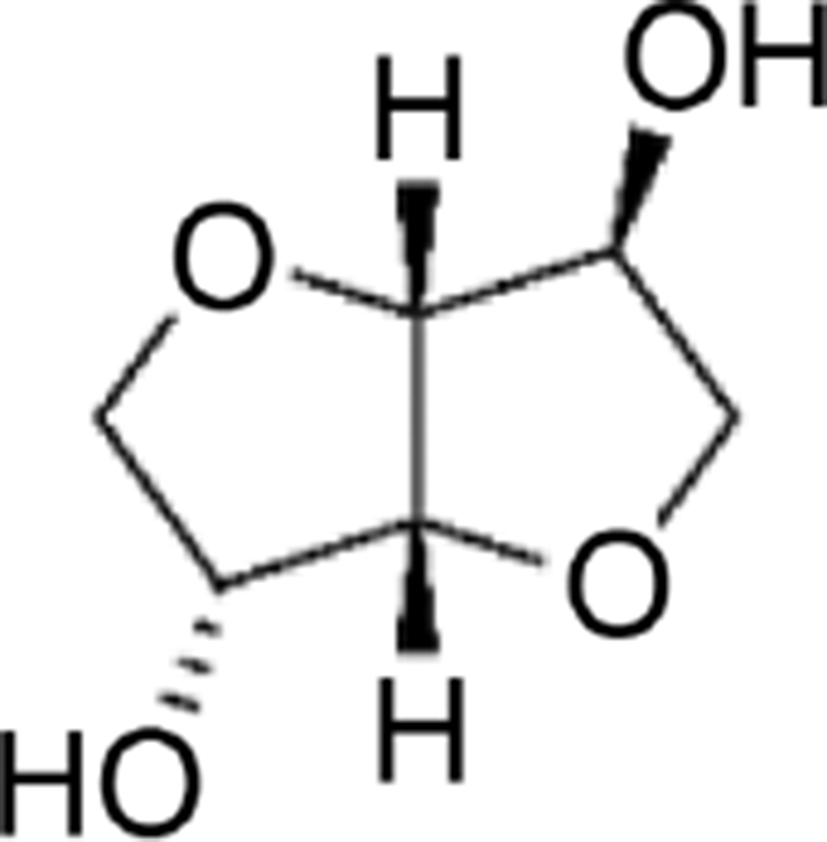
본 연구에서는 oleic acid의 오존 분해 방법으로 생산한 azelaic acid, 피마자유에서 추출한 sebacic acid를 사용하였다. Azelaic acid, sebacic acid 와 1,3-propanediol를 200°C 전후까지 온도를 상승시켜 에스테르화 반응을 진행시킨 후 감압하며 승온하여 에스테르화율을 높여 목표로 하는 분자량과 저 산가의 바이오 폴리에스터 폴리올을 만들었다. 에스테르화 반응 후, 폴리올을 사슬연장제(1,4-butanediol, 1,3-propanediol, isosorbide), 디이소시아네이트(MDI)와 1:1:1.1의 비율로 혼합하여 열가소성 폴리우레탄을 합성하였다. 사슬연장제 종류를 달리한 합성 공정에서 폴리우레탄의 화학 구조, 성분 및 분자량을 조사하였다. 기계적 물성에 있어 이들의 영향을 확인하였고, 또한 외부환경에 변화를 주기 전과 후의 인장강도 측정을 통해 이들의 내열성, 내수성, 내화학성을 비교하였다.
Experimental
Azelaic acid (Emerox 1117, Emery Olechemicals), sebacic acid (Arkema), 1,4-butanediol (1,4-BD, 99%, Daejung Co.), 1,3-propanediol (1,3-PD, 99%, TWSISChem), isosorbide (90%, Covestro Chemical) 그리고 4,4’-methylenebis phenyl isocyanate (MDI, 99%, Dongyang Chemical)를 Table 1에 나타내었다. 열가소성 폴리우레탄 합성에 사용한 폴리올은 60°C 열풍오븐에서 액상으로 융해시켜 사용하였고, 이소시아네이트 역시 냉동 보관한 MDI를 60°C 오븐에서 액상으로 융해시켜 사용하였다.
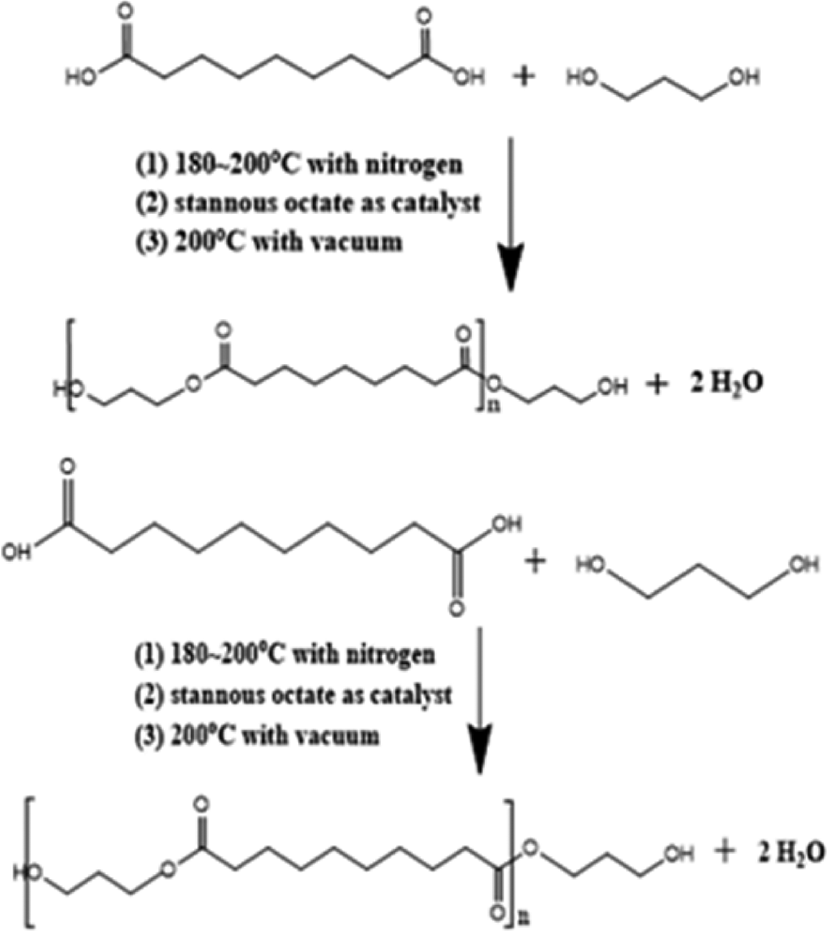
Azelaic acid, sebacic acid와 1,3-propanediol를 둥근 바닥 플라스크에 투입하고, 열을 가하면서 교반 및 질소 퍼지하였다. 160~190°C에서 2시간, 200°C에서 2시간 동안 교반시켰다. 생성물인 물이 어느정도 제거되면 촉매로 stannous octate를 넣어주었다. 이때, 교반 속도는 400 rpm, 칼럼 온도는 90~100°C 를 유지하였다. 반응률이 80%가 되면 질소를 제거하고, 저진공(40 torr)을 걸어 반응을 진행시켰다. 산가를 측정하여 1이하가 되면 고진공(2 torr)을 걸어 분자량을 조절한 후 60~70°C 로 냉각시키면 중합물을 얻을 수 있다.12,13 폴리에스터 폴리올 중합 반응을 Scheme 1에 나타내었다. 여기서 진공을 걸어주는 이유는 에스테르 평형 반응에서 생성물 중 하나인 물을 제거하여 정반응을 촉진하기 위해서이다.
폴리에스터 폴리올의 반응률을 측정하기 위해 ASTM D7253-06 (Standard test method for polyurethane raw material)에 따라서 산가를 측정하였다.14,15 산가 측정 방법은 시료 2 g을 정량하여 Methyl Ethyl Ketone (MEK)에 녹인 후, 페놀프탈레인 지시약을 넣고 0.1 N-KOH로 적정하여 아래의 식 (1)으로 계산한다.
A = 본 시험에 소비된 적정액의 부피(ml)
N = 0.1 N-KOH 수용액의 노르말 농도
W = 시료의 양(g)
폴리에스터 폴리올의 분자량을 측정하기 위해 말단기 정량법의 하나인 수산기가를 측정하였다.16 ASTM E222-10 (Standard test method for hydroxyl groups using acetic anhydride acetylation) 방법을 이용하였다. 수산기가 측정 방법은 아세틸화 시약을 폴리올과 반응시키고, 과잉의 산을 1 N-NaOH로 적정하여 아래의 식 (2)으로 계산한다.17
A = 공 시험에 소비된 적정액의 부피(ml)
B = 본 시험에 소비된 적정액의 부피(ml)
N = 1 N-NaOH 수용액의 노르말 농도
W = 시료의 양(g)
분자량은 수산기가를 구한 후 아래의 식 (3)으로 계산한다.18
폴리에스터 폴리올 제조 시 투여한 원료의 양 및 산가, 수산기가, 분자량을 Table 2에 나타내었다.
| Sample | Amount (g) | Acid value | OH value | Mw | ||
|---|---|---|---|---|---|---|
| Azelaic acid | Sebacic acid | 1,3 PD | ||||
| PE 1 | 167.57 | - | 101.39 | 1.63 | 106 | 1058 |
| PE 2 | - | 169.6 | 96.63 | 0.5 | 118.8 | 944 |
Table 3에 나타낸 것처럼 폴리에스터 폴리올, 사슬연장제, 이소시아네이트를 1:1:1.1의 비율로 주입한 후 교반하였다. 150~200 rpm으로 2~3분간 교반하고 테프론 시트에 부었다. 100°C 열풍오븐에서 6일간 보관하여 여분의 우레탄 반응을 유도하고, 5시간 상온에서 숙성하였다. 가열시편제작기(1008a, Ocean Science)를 사용하여 170°C에서 10 MPa의 압력으로 사각형의 최종 시편을 제작하고, 그 시편으로 분석을 시행하 였다.
폴리에스터 폴리올, 열가소성 폴리우레탄의 화학 구조를 푸리에 변환 적외선 분광법으로 조사하였다. 적외선 스펙트럼은 Perkin Elmer Spectrum 100® 로 64회 스캔하고, 4 cm−1의 해상도로 기록하였다. 스펙트럼의 파장 범위는 650~4000 cm−1 이었다.
열가소성 폴리우레탄의 열 중량 분석에 TA Instruments TGA Q500 V20을 사용하였다. 질소 분위기(200 ml/min) 하에서 10°C/min의 승온 속도로 온도 범위 30~800°C에서 분석하였다.
열가소성 폴리우레탄의 분자량은 겔 투과 크로마토그래피(Waters, USA, ACQUITY APC Core System) 분석에 의해 측정되었다. 시편 0.02 g을 DMF 1 g에 녹인 후 THF 9 g으로 희석하여 40분간 초음파 처리한 뒤 필터하여 분석하였다.
ASTM D412-A 규격의 아령형 틀을 사용하여 열가소성 폴리우레탄의 시편을 제작하였다. 이 시편을 UTM (AGS-X, SHIMADZU Inc.)을 사용하여 인장 속도 100 mm/min 으로 측정하였다.
열가소성 폴리우레탄 시편을 100°C 열풍 오븐에서 24시간 동안 노화시킨 후 UTM (AGS-X, SHIMADZU Inc.)을 사용하여 인장 속도 100 mm/min 으로 인장강도를 측정하였다.
열가소성 폴리우레탄 시편을 항온 항습기에서 일주일 간 70°C, 95%의 항온 항습 조건으로 보관한 후 UTM (AGS-X, SHIMADZU Inc.)을 사용하여 인장 속도 100 mm/min 으로 인장강도를 측정하였다.
열가소성 폴리우레탄 시편을 상온의 10% NaOH 용액에 7일간 침전시킨 후 UTM (AGS-X, SHIMADZU Inc.)을 사용하여 인장 속도 100 mm/min 으로 인장강도를 측정하였다.
열가소성 폴리우레탄의 경도는 Shore A 경도계(TIME, TH200)를 사용하여 ASTM D22-40에 따라 5회 측정 후 최대값과 최소값을 제외한 나머지를 평균하여 구하였다.
Results and Discussion
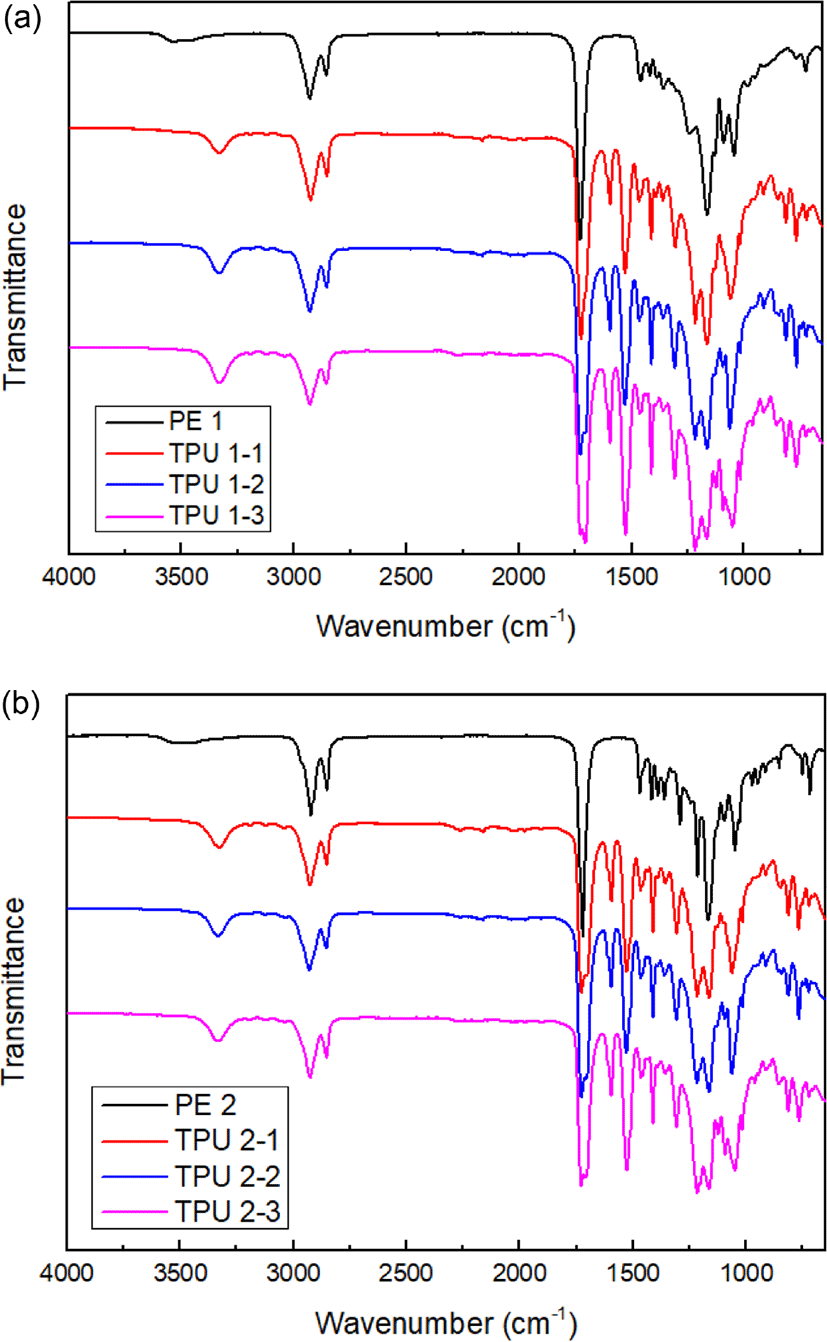
Figure 1(a), (b)에 bio-PE, bio-TPU의 FT-IR 분석 결과를 나타내었다. PE 곡선과 비교했을 때, 폴리우레탄의 전형적인 피크를 확인할 수 있다. 우레탄 그룹(-NHCOO)의 –NH 신축 진동은 3300 cm−1, -NH 변각 진동은 1530 cm−1 부근에 나타나고, >C=O 신축 진동은 1730 cm−1에서 나타난다. 3000-2840 cm−1 부근에서는 azelaic acid, sebacic acid의 C-H shoulder가 관찰되고, PE 곡선에서 1300-1000 cm−1 부근에서는 폴리올 성분에 따른 특징적 피크를 확인할 수 있다. 사슬연장제로 isosorbide를 사용한 TPU 1-3, 2-3 곡선을 보면, 1220 cm−1 (C-O 신축 진동) 피크가 1170 cm−1 (C-O 신축 진동) 보다 크게 나타난다. 방향족 디이소시아네이트의 벤젠 고리는 1600 cm−1에서 관찰된다.
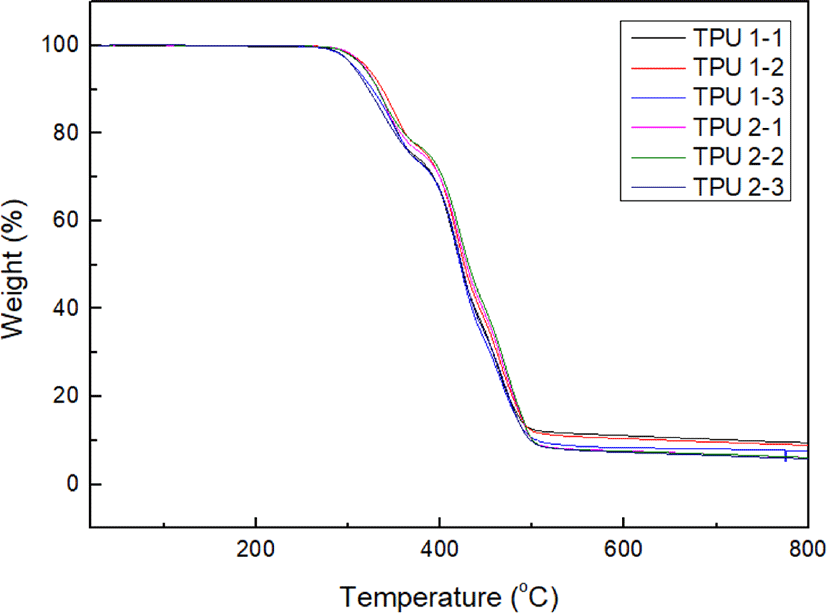
Figure 2, 3에 TGA 분석 결과를 나타내었다. Isosorbide를 사용한 TPU 1-3, 2-3의 초기 열분해 온도는 약 260°C로 다른 TPU에 비해 20°C 정도 낮았다. 또한 가장 큰 중량 손실을 보이는 두 번째 곡선에서 TPU 1-3, 2-3의 퍼센트(%)가 가장 높은 것으로 보아 isosorbide의 입체 구조로 인해 충진성이 낮아 열에 대한 저항성 또한 낮음을 알 수 있다. 우레탄은 3단계에 걸쳐 분해가 일어나는데, 이는 우레탄 그룹의 분해가 먼저 일어난 후 소프트 세그먼트의 분해가 일어나기 때문이다.18
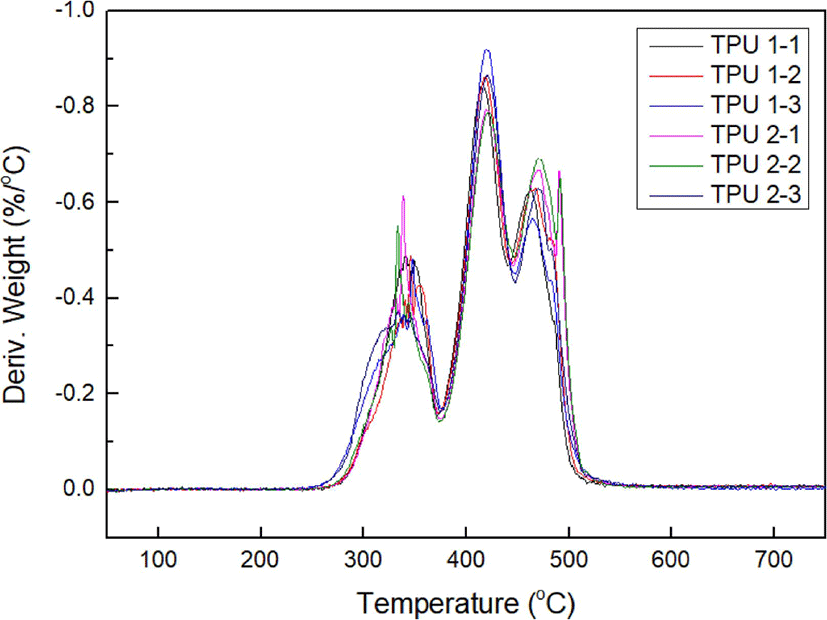
Table 4는 GPC를 통한 분자량 측정 결과이다. 산으로 sebacic acid를 사용한 TPU 2의 분자량이 TPU 1에 비해 크게 나타났다. 그 중에서도 사슬연장제로 isosorbide를 사용한 TPU 1-3, 2-3의 분자량이 상대적으로 크고, 비교적 좁은 분자량을 분포를 가졌다.
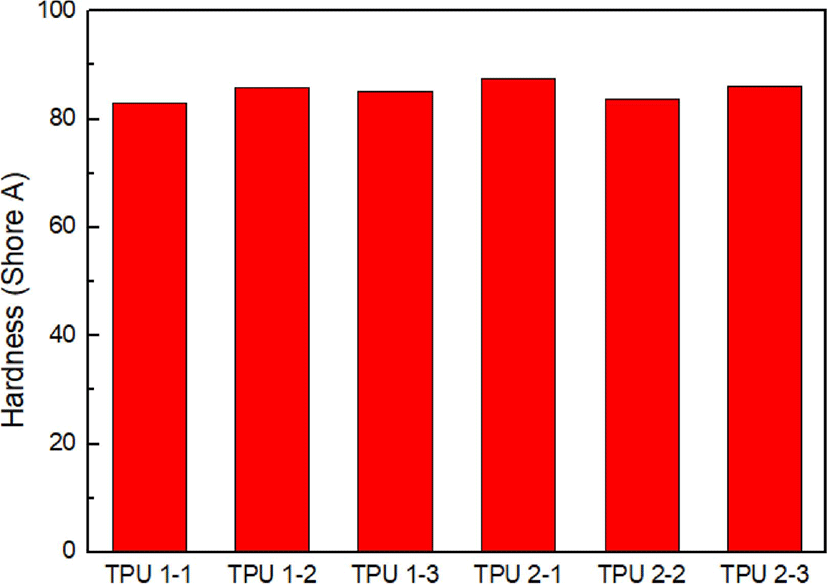
Figure 4는 경도의 결과이다. 제조한 TPU 모두 80 이상으로 높은 경도 값을 나타낸다. 이는 사슬연장체 첨가로 하드세그먼트가 증가해 경도 또한 증가했음을 알 수 있다.
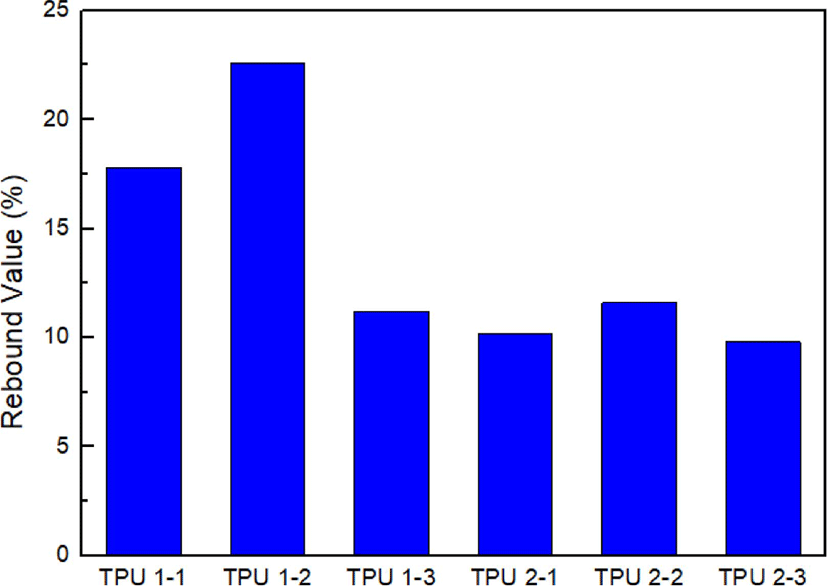
반발탄성률을 Figure 5에 나타내었다. 산으로 azelaic acid를 사용한 TPU 1-1~3의 탄성률이 더 높았다. 이는 azelaic acid의 메틸렌기가 홀수이므로 conformation 에너지가 높은 반면 응집에너지가 낮아 탄성이 좋기 때문이다.19 그 중에서도 사슬연장제로 메틸렌기가 홀수인 1,3-PD를 사용한 TPU 1-2, 2-2의 탄성이 가장 좋았다. 한편, 입체적이고 단단한 화학구조를 가진 isosorbide를 사용한 TPU 1-3, 2-3의 탄성률이 가장 낮았다.
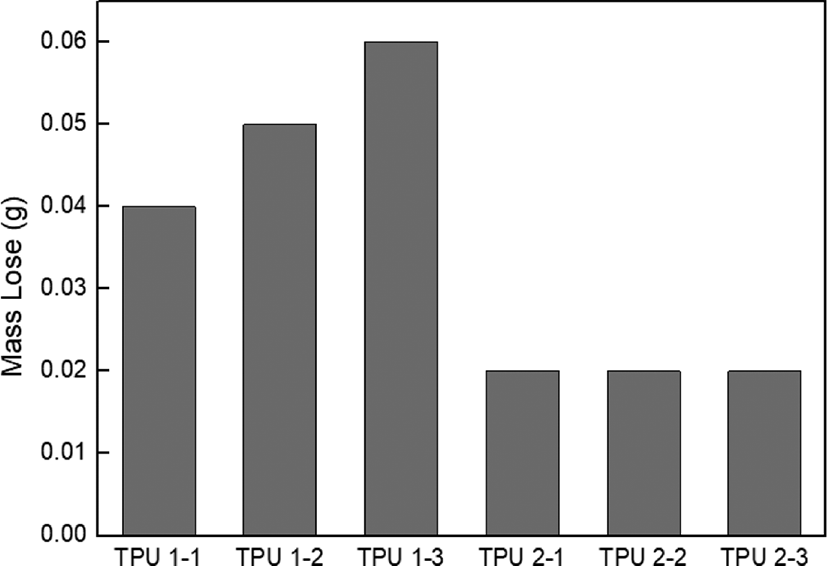
Figure 6에 내마모성 테스트 결과를 나타내었다. Sebacic acid를 사용하여 제조한 TPU 2-1~3의 질량 손실이 적은 것으로 보아 내마모성이 우수함을 확인하였다. 이는 메틸렌기가 짝수로 conformation 에너지가 낮아 결정을 이루고, 그로 인해 응집력이 좋기 때문이다. 한편, isosorbide를 사용한 TPU 1-3은 가장 취약한 내마모성을 보였다. 이것은 isosorbide 가 폴리올을 형성할 때 입체 장애로 인하여 고분자 사슬의 운동을 방해하여 점도가 높아지고, 우레탄 생성 후에도 여전히 분자의 운동성이 낮아 깨어지는 물성을 갖고 있기 때문이다.
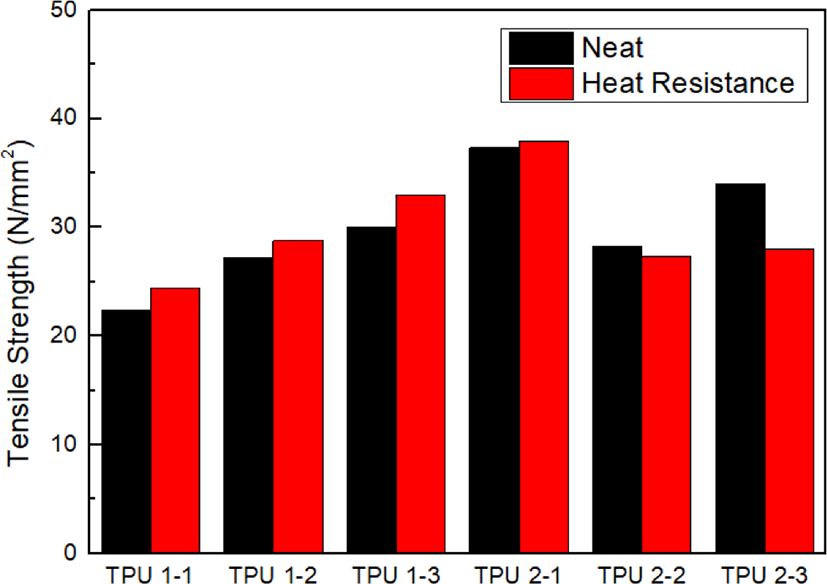
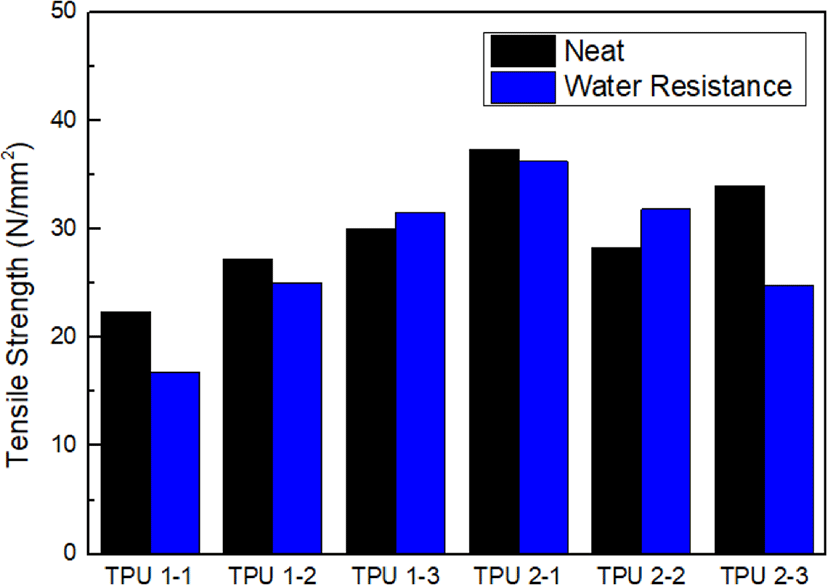
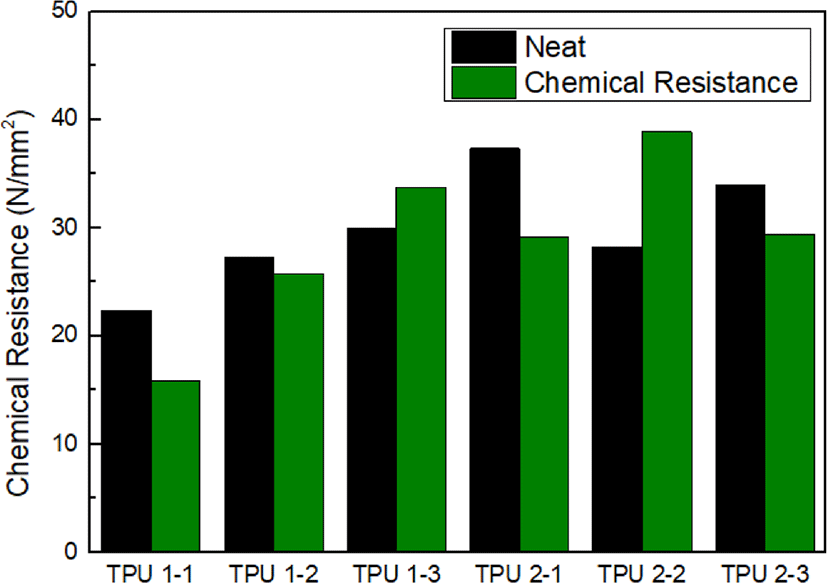
Figure 7, 8, 9는 아무 처리하지 않은 TPU의 인장강도와 열 처리, 내화학성 처리, 내수성 처리 후의 인장강도를 비교한 그래프이다. 우선 산으로 sebacic acid를 사용한 TPU 2의 인장강도가 TPU 1에 비해 높았다. 그 중에서도 메틸렌기가 짝수인 sebacic acid와 1,4-BD가 결합한 TPU 2-1의 인장강도가 가장 좋았다. 이는 메틸렌기가 짝수일 경우 구조적으로 안정해 물성이 좋아짐을 알 수 있다. Figure 7에서 열처리 후 TPU의 인장강도는 TPU 2-3을 제외하고는 증가하거나 거의 일정함을 확인할 수 있다. 사슬연장제 첨가로 하드세그먼트의 함량이 증가하여 내열성이 향상되었음을 알 수 있다. 반면 내화학성, 내수성 측면에서는 물성이 떨어짐을 확인했는데, TPU 1-3, 2-2는 상대적으로 우수한 내화학성, 내수성을 나타내었다.
Conclusions
지방산인 oleic acid의 오존 분해 방법으로 생산한 azelaic acid, 피마자유에서 추출한 sebacic acid와 옥수수당을 발효하여 생산한 1,3-propanediol 으로 바이오 폴리에스터 폴리올을 합성하였다. 여기에 다양한 사슬연장제(1,3-PD, 1,4-BD, iso- sorbide)와 MDI를 첨가하여 폴리우레탄을 제조함으로써 사슬 연장제 종류에 따른 폴리우레탄의 물성을 비교하였다.
산으로 sebacic acid를 사용한 TPU 2는 TPU 1과 비교해 분자량, 내마모성, 인장강도에서 우수한 물성을 보였다. 산으로 azelaic acid를 사용한 TPU 1은 우수한 탄성을 나타냈다. 이는 메틸렌기가 짝수이면 응집력이 좋아 결정성이 높기 때문에 경도, 내마모성, 인장강도가 우수하고, 메텔렌기가 홀수이면 응집력이 떨어져 비결정성을 나타내어 탄성이 좋아지는 특성 때문이다. 그 중에서도 사슬연장제로 메틸렌기가 짝수인 1,4-BD를 사용한 TPU 2-1의 인장강도가 가장 높았고, 메틸렌기가 홀수인 1,3-PD를 사용한 TPU 1-2는 탄성이 가장 뛰어났다. 한편 isosorbide를 사용하였을 때는 입체적이면서 산소를 더 많이 함유한 독특한 구조로 인해 열 안정성, 내마모성에서 취약한 물성을 보인 반면, 높은 인장강도를 나타내었고, TPU 1-3의 경우 우수한 내수성, 내화학성을 나타내었다.