Review
A Concise Review of Recent Application Progress and Future Prospects for Lignin as Biomass Utilization
Seo-Hwa Hong1, Seok-Ho Hwang1,†
1Materials Chemistry & Engineering Laboratory, School of Polymer Science & Engineering, Dankook University, Yongin, Gyeonggi-do 16890, Republic of Korea
© Copyright 2021 The Rubber Society of Korea. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Aug 17, 2021; Revised: Aug 20, 2021; Accepted: Aug 24, 2021
Published Online: Sep 30, 2021
Abstract
Biomass lignin, a waste produced during the paper and bio-ethanol production process, is a cheap material that is available in large quantities. Thus, the interest in the valorization of biomass lignin has been increasing in industrial and academic areas. Over the years, lignin has been predominantly burnt as fuel to run pulping plants. However, less than 2% of the available lignin has been utilized for producing specialty chemicals, such as dispersants, adhesives, surfactants, and other value-added products. The development of value-added lignin-derived co-products should help make second generation biorefineries and the paper industry more profitable by valorizing lignin. Another possible approach towards value-added applications is using lignin as a component in plastics. However, blending lignin with polymers is not simple because the polarity of lignin molecules results in strong self-interactions. Therefore, achieving indepth insights on lignin characteristics and structure will help in accelerating the development of lignin-based products. Considering the multipurpose characteristics of lignin for producing value-added products, this review will shed light on the potential applications of lignin and lignin-based derivatives on polymeric composite production. Moreover, the challenges in lignin valorization will be addressed.
Keywords: lignin; applications; fine chemicals; filler; composite
Introduction
최근 플라스틱 폐기물의 급격한 증가에 따른 지구 환경오염 문제로 인해 바이오 기반 재료 또는 생분해성 고분자의 중요성이 날로 증가하고 있다. 일반적으로 지구 온난화의 주범으로서 지적되고 있는 화석연료의 사용은 범 세계적으로 환경 규제가 강화되고 있기 때문에 석유 자원을 대체하여 지속적인 사용과 개발이 가능한 환경친화적인 재료의 사용은 필수적인 시대가 도래 하였다. 이러한 시류에 부합하고 재생가능한 자원으로서, 바이오 플라스틱에 대한 연구개발이 활발하게 진행되어 오고 있다. 주로 2세대 바이오매스인 전분이나 옥수수에서 추출한 단량체(monomer)를 기반으로 중합된 PLA [Poly(lactic acid)], 미생물에 의한 발효공정에서 생산 가능한 PHB [Poly(hydroxybutyrate)]가 현재까지 가장 생분해도가 높은 중합체들로 알려져 있으며, 석유기반 단량체를 기반으로 중합된 PBAT [Poly(butylene adipate-co-terephthalate)] 또는 PBS [Poly(butylene succinate)] 등과 같은 생분해성 고분자에 대한 연구개발도 다양하게 이뤄지고 있다.1 하지만, 생분해성 고분자 물성이 기존 석유기반 고분자 대비 많이 떨어지는 단점이 존재하기 때문에 다양한 산업군에 적용되기엔 현재까지 많은 제약이 따른다.
이러한 제약을 극복하기 위해 바이오 플라스틱 내에 강화제로 유리섬유, 무기입자, 합성섬유 등을 첨가시키는 복합화가 시도되고 있다.2 그럼에도 불구하고, 이와 같은 강화제도 분해되지 않는 특성으로 인해 결국 환경오염을 초래하는 미세 플라스틱으로 잔류하는 문제가 발생하게 된다. 따라서, 환경 오염의 부하를 줄이고, 지속가능한 강화 재료로 목질계 섬유를 사용하는 것은 다양한 이점을 제공할 수 있다. 목질계 섬유는 재생이 가능하고, 값이 저렴하며, 밀도가 낮은 특성 때문에 경쟁력 있는 복합재를 만들 수 있으며, 현재 사용되고 있는 목질계 섬유로는 볏짚, 대마, 케나프, 밀짚 등과 같은 섬유가 널리 사용되고 있다.3,4 하지만 이런 목질계 섬유는 친수성이 강하고 높은 뭉침 특성으로 인해 계면 접착력의 제약으로 인해 고분자 매트릭스와 이종 계면을 형성하여 수분에 취약한 특성을 나타낸다. 결과적으로 생분해성 강화재료의 표면을 목적에 맞게 개질하여 고분자 매트릭스와 접목시키는 것은 필수적이고, 안정적인 성능 유지를 가능하게 할 수 있다.5
기존에 사용되는 대부분의 목질계 섬유 성분은 셀룰로오스를 주로 사용하고 셀룰로오스와 화학적으로 연결되어 있는 리그닌을 제거하여 사용해 왔다. 리그닌을 제거하는 과정에서 대량의 폐수가 발생하고, 공정 비용이 발생하기 때문에 부산물로 얻어지는 리그닌을 보다 효율적으로 사용하고자 하는 연구가 진행되기 시작하였다.6 리그닌은 지구상에 있는 셀룰로오스 소재 다음으로 풍부한 바이오 폴리머로 제지 산업에서 발생하는 부산물로서 대량의 목재 폐기물로 볼 수 있다. 연간 약 7천 만톤에 이르는 많은 양의 리그닌을 재사용하기 위해 다양한 연구 개발이 수행되고 있다.5,7-9 산업혁명 전후 가죽 염색 재료로 사용되었다가 점차적으로 시멘트와 아스팔트, 콘크리트 등의 도로 포장재의 안정제로 활용이 확대되었다. 근래에 들어, 리그닌의 화학개질을 통해 친환경 화학소재인 원료로서 활용성이 크게 대두되고 있다. 2008년 독일 Tecnaro사는 리그닌을 이용하여 친환경 바이오 플라스틱인 Arboform을 제품화하였다.
페놀성 화합물인 리그닌은 우수한 기계적 특성, 항산화성, 생분해성 등으로 인해 고분자와 블렌드하여 바이오 복합재를 만들어 지속가능한 플라스틱 사용을 도모하는 연구들이 활발히 진행되고 있다.9,10 여기서 리그닌을 활용한 최근 기술 개발 동향과 산업적 응용 분야를 전망하고자 한다.
리그닌의 화학 구조와 종류
1. 리그닌의 일반적 특성
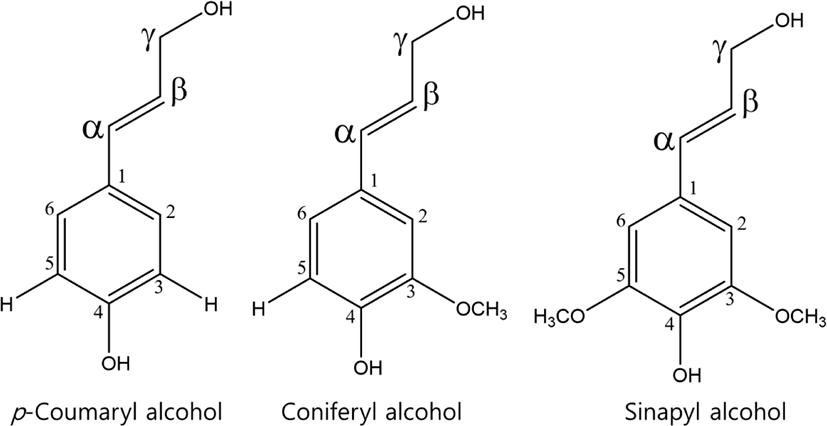
목재의 주요 구성 성분은 크게 리그닌, 셀룰로오스, 헤미셀룰로오스로 나뉠 수 있다. 그 중에서 리그닌은 약 25~30% 이상을 차지하고 있으며, 리그닌의 화학구조를 살펴보면 다양한 관능기를 포함하고 있다. 리그닌은 실제로 식물 세포벽에 존재하며 주로 3가지 주요 페닐프로판(phenyl propane) 단위인 coniferyl alcohol (guaiacyl, G units), p-coumaryl alcohol (p-hydroxyphenyl, H units), 그리고 sinapyl alcohol (syringyl, S units) 단량체들이 3차원 망상구조를 형성하고 있다(Figure 1).
리그닌은 세포벽에서 셀룰로오스와 헤미셀룰로오스를 보호하고 지지해주는 형태로, 세포벽 최외각에 존재하고 있다. 일반적으로 침엽수 목재(softwood)에선 25~30% (G units), 활엽수 목재(hardwood)는 16~24% (G & S units), 일년생 초목 (grasses) 13~18% (G, S & H units)로 식물 유형에 따라 리그닌 함량이 다양하게 존재한다.12-14 목재로부터 리그닌을 분리해내기 위해 리그닌 내 수많은 탄소-탄소 결합을 절단해야하며 이때, 많은 에너지를 필요로 하며 화학적 처리를 거치는 펄프화 공정인 경우, 리그닌 내 대부분 탄소-탄소 결합은 유지되고 있으며, S 단위의 메톡시 그룹의 입체 장애 효과로 인해 가교된 탄소-탄소 결합 구조와 가지구조(branching)를 형성할 가능성이 적다. 따라서 활엽수 목재는 일반적으로 침엽수 목재에 비해 탄소-탄소 결합이 적게 구성되어 있다(Table 1). 산업에서 추출되는 리그닌의 분자량은 약 1,000~20,000 g/mol이며, 리그닌 물성에 영향을 미치는 변수로 유리전이온도 (glass transition temperature; Tg)가 중요하다. 대부분의 Tg 범위로는 100~170°C 부근이며, 페놀성 하이드록시기를 갖는 구조에서 수소결합에 의한 결합 정도가 리그닌의 유리전이온도가 결정한다.15-17
Table 1.
Common Linkages in Lignin and Their Presence in Softwood and Hardwood
|
Type |
Bonds |
Frequency in softwood (%) |
Frequency in hardwood (%) |
|
β-aryl-ether |
β-O-4’ |
35-60 |
50-70 |
|
Diaryl ether |
4-O-5’ |
< 4 |
~7 |
|
Dihydroxy biphenyl |
5-5’ |
10 |
~5 |
|
Phenyl coumarane |
β-5’ |
11-12 |
4-9 |
|
Pinoresinol |
β-β’ |
2-3 |
3-4 |
Download Excel Table
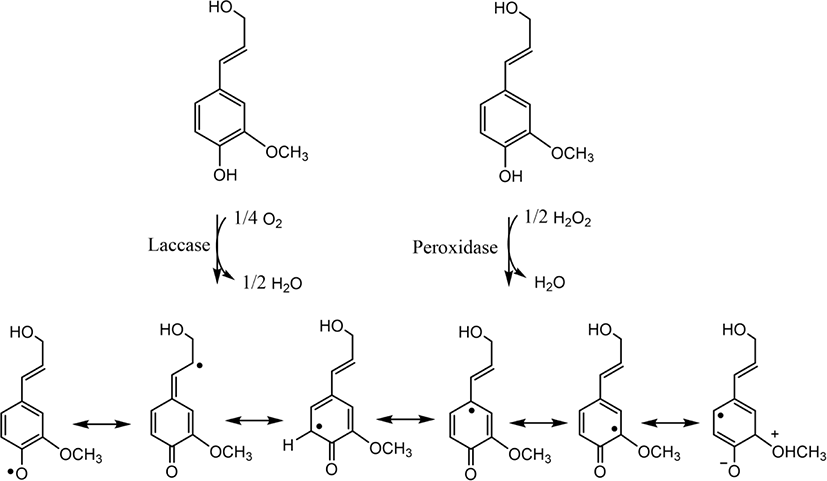
리그닌은 목재 내부에서 모노리그놀(monolignol)로부터 탈수소화(dehydrogenation) 반응에 이은 중합반응 과정을 통해 합성된다(Figure 2). 퍼옥시다아제(peroxidases), 락카아제 (laccases), 폴리페놀 옥시다아제(polyphenol oxidases) 같은 효소들은 모노리그놀을 모노리그놀 라디칼로 변환시키는 탈수소화 반응을 담당한다. 비록 정확한 메커니즘은 규명되지 않았지만, 퍼옥시다아제와 락카아제는 과산화수소(H2O2)와 산소를 산화제로 이용하여 모노리그놀을 산화시킨 후, 공명 안정화된 모노리그놀 라디칼 형성에 관여한다. 짝을 이루지 않은 홀전자(unpaired electron)는 다른 단량체 라디칼에서 홀전자를 받아 리그닌 내에 새로운 공유결합을 형성한다. 페닐 프로판 구조의 라디칼들은 서로 커플링 반응을 통해 거대 고분자들이 형성되는 것으로 알려져 있다. 페놀성 하이드록시기가 앞서 언급한 효소에 의한 반응이 진행될 때, 이웃한 페닐 프로판 구조 단량체와 에테르 결합을 형성하게 된다.19 이때, 리그닌의 거대 고분자 축합체 형성은 특성상 5가지의 형태의 안정화된 라디칼 공명구조들이 존재한다. 라디칼 공명구조들이 서로 라디칼 커플링 반응에 의해 이량체(dimer)가 되고, 다른 라디칼 단량체와 커플링되어 삼량체(trimer)가 되고, 계속해서 라디칼 단량체와 반응하여 3차원적 무정형인 거대 고분자 망상구조를 형성하게 된다.
일반적으로 리그닌에서 가장 많이 이루어진 결합은 β-O-4 (β-O-4-aryl ether) 결합이다. 그 외에 다른 주요 결합은 α-O-4 (α-O-4-aryl ether), β-5 (β-5-phenylcoumaram), 5-5 (5-5-biphenyl), 4-O-5 (4-O-5-diaryl ether), β-1 (β-1-(1,2-diarylpropane)) 및 β-β (β-β-resinol) 결합 등이 존재한다. 리그닌은 부가가치 제품을 생산하기 위해 적용될 수 있는 다양한 특성을 가지고 있으나, 리그닌 구조의 이질성으로 인해 목표 제품으로 분해 및 분리정제 되기가 매우 어렵다. 리그닌 구조의 복잡성과 전처리 과정의 효과로 인해 리그닌으로부터 화학 물질을 식별하고 추출하는 데는 리그닌의 고분자적 특성, 결합 및 방향족 고리에 연결된 관능기의 성질을 반드시 확인해야 한다.
2. 리그닌의 종류
2.1 소다 리그닌(Soda lignin)
소다 리그닌은 밀짚과 사탕수수와 같은 비목질계 바이오매스를 주원료로 사용하는 소다 펄프공정(soda pulping process)의 부산물로 얻어진다. 이 공정은 무황 공정으로 알려져 있으며, 크래프트 공정(kraft pulping process)에 비해 큰 장점이 있다.20 공정상에서 알카리 전처리에는 암모니아, 수산화 나트륨, 수산화 칼륨 등이 사용될 수 있으며, 대부분 13~16% 수산화 나트륨(pH 11~13)이 주로 사용된다. 수산화 나트륨은 강력한 염기 촉매 중 하나로 알카리 전처리 공정에서 가장 가수분해 효과가 크다. 이때, 리그닌을 분리하는 방법으로 산 (acid)을 이용한 침전방법이 적용되고 있다. 다른 알카리 공정과 달리 압력과 온도(140~170°C)가 낮은 편이지만, 강염기이기 때문에 부식되는 속도가 빠르다. 수산화 나트륨은 수산화 이온(−OH)과 나트륨 이온(Na+)으로 해리되며 수산화 이온 농도가 증가함에 따라 가수분해 속도가 증가한다. 이에 따라 페놀이 제거되는데, 이 과정에서 α-O-4 ether와 β-O-4 ether 결합이 절단된다.21
이러한 소다 펄프공정은 다른 리그닌 추출 방법에 비해 환경에 미치는 영향이 낮다고 보고되었다.20,22 소다 리그닌은 사탕수수, 아마, 짚과 같은 작물이 주로 공정에 사용되기 때문에 질소와 실리카를 포함할 수 있다. 따라서, 비목재에서 소다 리그닌을 회수하면 높은 실리카 함량이 리그닌과 함께 침전되어 리그닌 순도와 품질이 저하될 수 있다. 소다 리그닌의 불순물은 0.7~2.3 wt.% 회분, 1.5~3.0 wt.% 당(sugar), 2.5~5.0 wt.% 수분이며 황 원소를 포함하지 않는다(Table 2).20,23 목재가 아닌 원료에서 얻은 소다 리그닌은 유리전이온도가 낮고 페놀성 하이드록시기 함량이 높은 것으로 보고되었다.24 그럼에도 불구하고, 소다 리그닌의 열적 거동은 불순물(회분 및 당)에 따라 달라지는데, 이러한 불순물은 가소제 또는 가소제 역할을 수행하는 것으로 보고되고 있다.24,25
Table 2.
Chemical and Physical Properties of Different Commercial Lignin
|
Type |
Sulfur content (wt.%) |
Sugar content (wt.%) |
MW (g/mol) |
Ash content (wt.%) |
Moisture content (wt.%) |
PDI |
Purity |
Elemental analysis |
Tg (°C) |
|
N (wt.%) |
H (wt.%) |
C (wt.%) |
|
Kraft lignin |
1.0-3.0 |
1.0-0.23 |
< 25,000 |
0.5-3.0 |
3.6-6.0 |
2.5-4.0 |
High |
0.9 |
5.8 |
62.8 |
108-165 |
|
Lignosulfonate |
3.5-8.0 |
- |
< 15,000 |
4.5-8.0 |
5.8 |
4.2-9.0 |
Low |
0.2 |
3.7 |
47.9 |
127-154 |
|
Soda lignin |
0 |
1.5-3.0 |
< 15,000 |
0.7-2.3 |
2.5-5.0 |
2.5-3.5 |
Medium-high |
0.9 |
5.9 |
61.9 |
150-155 |
|
Organosolv lignin |
0 |
1.0-3.0 |
< 5,000 |
~1.7 |
7.5 |
1.5-2.4 |
Very high |
0.3 |
5.9 |
61.1 |
89-97 |
Download Excel Table
소다 펄프공정에 사용되는 원료 공급원은 소다 리그닌의 열적 거동에도 영향을 미칠 수 있다. 예를 들어 밀짚에서 얻은 소다 리그닌은 대마에서 얻은 소다 리그닌보다 높은 Tg 값을 가지며 약 15,000 g/mol 미만의 분자량을 가지는 것으로 보고되었다.26-28 소다 리그닌은 방향족 화합물과 낮은 몰질량을 갖는 페놀 생산으로 주목을 받고 있다.29 또한 소다 리그닌은 동물 영양제 및 페놀 수지와 같은 용도에 더 적합한 것으로 보고되고 있다. 이러한 용도는 고순도 리그닌을 필요로 하기 때문이다.30 크래프트 리그닌(kraft lignin) 및 리그노술포네이트(lignosulfonate)와 같은 대부분의 리그닌 유형에서 리그닌에 화학적 결합으로 존재하는 황 원소를 제거하는 것은 상당히 어렵고, 많은 비용을 초래한다. 반면에 소다 리그닌은 황 원소를 포함하지 않기 때문에 다른 펄프공정보다 이 펄프공정이 황 원소를 포함하지 않는 리그닌을 얻는데 유리할 수 있다. 전반적으로 소다 리그닌이 불용성 물질로 응용되고 있지만, 크래프트 리그닌의 응용 범위를 확장하기 위해 화학적으로 개질되어 사용될 수 있다.
2.2 크라프트 리그닌(Kraft lignin)
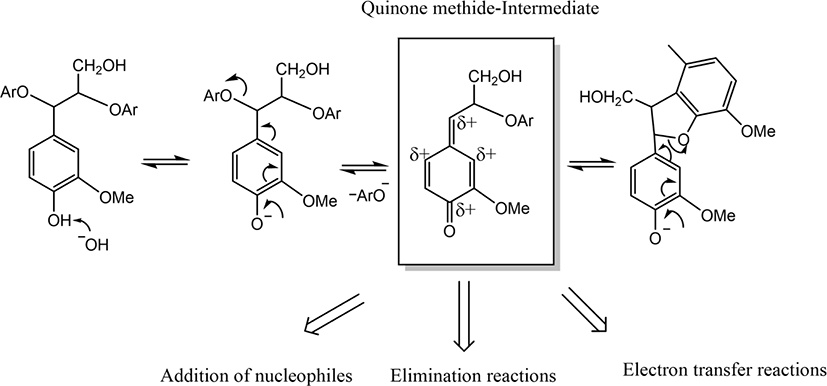
크래프트 리그닌을 추출하기 위한 크래프트 공정(kraft pulping process)은 소다 펄프공정을 보완한 공정으로, 리그닌을 추출하기 위하여 수산화나트륨 뿐만 아니라 황화나트륨 (Na2S)이 함께 사용된다. 알칼리성 분위기에서 리그닌 거대분자의 분해는 β-aryl ether 구조와 유사한 para-quinone methide이라는 중간체의 형성 과정을 포함하게 된다(Figure 3). 이 중간체는 페놀 그룹의 이온화와 α 위치에서 아릴 그룹과 비닐계 β-elimination 반응을 통해 형성된다. 생성된 중간체는 전자가 부족하며, 세 가지 다른 반응 메커니즘, 즉 친핵체 추가 (황화수소 음이온에 의한 친핵성 공격), 제거 반응, 탈 리그닌화를 촉진하기 위한 전자 전달 반응을 거치게 된다. 이후, 얻어진 흑액(black liquor)에는 다량의 리그닌이 함유하게 되며, 이를 농축하고 더 이상의 정제과정 없이 소각하여 펄프공정에 필요한 에너지원으로 주로 사용되어 왔었다.30
Figure 3.
The formation of para-quinone methide and its subsequent reaction mechanisms to delignification.30
Download Original Figure
크래프트 리그닌은 흑액을 산성화시켜 펄프공정에 사용한 약품과 헤미셀룰로오스를 분리하여 회수할 수 있다. 크라프트 공정에서 흑액을 산성화시키기 위해 두 단계로 수행되는데, 첫 번째 단계에서는 펄프공정 보일러에서 발생되는 고온의 폐가스나 석회 소성로에서 나오는 이산화탄소를 사용하여 흑액의 pH 값을 12에서 9~10 정도로 낮춘다. 크라프트 리그닌의 약 3/4이 이 단계에서 나트륨염 상태로 침전된다. 크래프트 리그닌은 높은 다분산지수(PDI), 높은 함량의 페놀성 수산기 및 소량의 황 원소를 포함하는 것으로 알려져 있다. 크래프트 리그닌은 화학 구조의 친수성 그룹이 부족하기 때문에 중성 및 산성 pH에서 물에 불용성이며, 2,000~3,000 범위의 수평균 분자량을 지니고 리그노술포네이트 보다 다분산성이 적다고 알려져 있다. 복잡한 구조와 낮은 수용성에도 불구하고,31-33 β-aryl의 절단을 통해 생성되는 높은 페놀성 하이드록시기 함량을 가진 크래프트 리그닌은 다양한 화학적 개질에 적합하다.
최근 몇 년 동안, 크라프트 리그닌이 점점 더 상업적으로 이용 가능해짐에 따라 크라프트 리그닌에 대한 연구도 함께 확대 적용되고 있다. 상업적으로 생산된 활엽수 혹은 침엽수 유래 크래프트 리그닌의 비교에서 침엽수 유래 크래프트 리그닌이 더 높은 페놀 하이드록시기와 페놀 고리에서 좀 더 자유로운 오르소(-ortho) 위치를 가지고 있다. 이러한 구조적 이점은 크래프트 리그닌의 아민화 및 카르복시 알킬화와 같은 화학적 개질이 가능하게 할 수 있다. 또한, 리그닌의 페놀성 하이드록시기에 도입 시 입체 장애 효과 때문에 리그닌 내 메톡시 그룹 함량이 중요하다.34 이는 아민화 및 카르복시 알킬화와 같은 반응이나 리그닌의 페놀성 히드록시기를 표적으로 하는 다른 반응에서도 매우 중요하다. 입체 장애 효과가 증가할수록 개질을 위한 시약과 상호 작용하는 페놀성 하이드록시기의 친화력을 감소시킨다. 다시말해, 가장 많은 양의 시나필 알코올 단위(더 높은 메톡시 그룹)를 함유하는 활엽수 기반 리그닌은 페놀성 히드록시기에 대한 입체 장애가 높아 침엽수 기반 리그닌에 비해 반응 효율이 감소하게 된다.
크래프트 리그닌은 알칼리 수용액(pH > 10.5), dioxane, acetone, dimethylformamide, 2-methoxyethanol 등에 용해되고, 대부분의 크래프트 리그닌은 셀룰로오스 생산 과정에 에너지원으로 재활용되기 위해 태워지며, 시중에서 쉽게 구할 수는 없다.33 일반적으로, 흑액의 연료 가치가 상대적으로 높기 때문에 크래프트 리그닌 제품은 일반적으로 고가 응용 분야에 사용되고 있다. 많은 응용 분야들에서 사용되는 기본 리그닌은 사용하기 전에 술폰화 또는 산화과정을 거친 후에 사용한다. 일단, 화학적 처리가 되면 크래프트 리그닌은 리그노술포네이트가 사용되는 응용 분야에 사용될 수 있다. 유화제나 유화 안정제, 격리제, 살충제 분산제, 염료 분산제, 알칼리성 세정제제의 첨가제, 미량 영양소 제제의 착화제, 응집제 및 페놀계 접착제의 증량제가 있으며, 또한 증량제나 개질제 및 고무 컴파운딩의 강화 안료로도 사용할 수 있다. 에톡실화 (ethoxylation)를 통해 개질된 술폰화 크래프트 리그닌은 최근 살충제 및 염료를 포함한 다양한 응용 분야에서 분산제로 사용되고 있다.34,35
2.3 리그노술포네이트(Lignosulfonate)
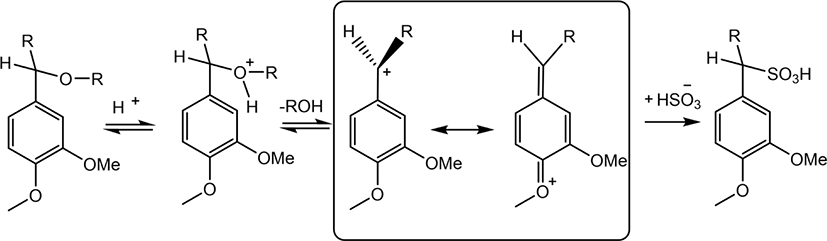
설파이트 펄프공정(sulfite pulping process)에서 목재 내 리그닌은 주로 페닐 프로판 단위의 측쇄에 있는 벤질 알코올, 벤질 아릴 에테르 및 벤질 알킬 에테르 결합에서 설폰화에 의해 용해된다. 일부 탈메틸화(dimethylation)는 중성 및 알칼리성 아황산염 펄프공정 중에도 발생하여 카테콜(catechol)과 메탄 술폰산(methanesulfonic acid)이 형성된다(Figure 4). 펄프 공정의 유형에 따라 칼슘, 나트륨, 마그네슘, 암모늄 리그노술포네이트 등 다양한 염의 형태인 리그노술포네이트를 얻을 수 있다. 흑액으로부터 리그노술포네이트를 분리하고, 정제하기 위한 다양한 방법이 개발되어 왔다. 초창기부터 가장 널리 사용된 공정 중에 하나는 과량의 석회를 첨가하여 사용된 흑액에서 칼슘 리그노술포네이트가 침전되어 90~95%의 리그닌을 회수할 수 있는 Howard 공정이다. 산업적으로 사용되고 있는 다른 방법으로는 한외 여과(ultrafiltration) 및 이온 배제(ion exclusion)가 있으며 이 방법은 이온 교환 수지를 사용하여 혼합용액으로부터 당과 리그닌을 분리한다. 리그노술포네이트를 분리하기 위한 실험적 방법에는 투석(dialysis), 전기 투석 (electrodialysis), 이온 배제, 알코올에 침전시키기 및 아민으로 추출하는 방법 등이 있다.22
리그노술포네이트의 큰 특징은 주로 리그닌의 지방족 부분에 부착된 친수성인 설폰산 그룹으로 인해 리그노술포네이트가 물에 용해된다는 점이다.31,33 그러나 설포네이트 그룹의 존재는 리그노술포네이트로부터 순수한 방향족 화합물 생산 가능성을 방해하는 것으로 보고되었다.36 리그노술포네이트는 상업적으로 이용 가능하지만, 크래프트 리그닌에 비해 더 많은 황 원소, 탄수화물 및 무기 불순물을 포함하기 때문에 상대적으로 순도가 낮다.37 리그노술포네이트의 황 원소 및 회분 함량은 저분자량 화합물(지방족 산 또는 바닐린 등) 및 고분자 합성20,38과 같은 일부 응용 분야에서 중요한 요소이다. 리그노술포네이트의 높은 회분 함량은 촉매 독으로 작용하여 화학적 변형 수율을 감소시킬 수 있다.39 게다가, 리그노술포네이트에 함유된 황 원소 함량이 높으면 복합재의 수분 흡수를 증가시켜 생분해를 촉진하기 때문에 리그닌 기반 복합재의 단점으로 작용할 수 있다.40 따라서 리그노술포네이트의 황 원소 함량은 그 적용 범위를 확대하기 위해 감소되어야 한다.41 하지만, 리그노술포네이트의 품질을 개선하기 위해 막 투석을 사용하여 선택적으로 정제하거나 분류하는 것은 매우 어렵다.42
리그노술포네이트는 수용성이기 때문에 대부분의 개질 반응은 수성 매질에서 수행된다. 리그노술포네이트의 음전하 밀도로 인해 폴리머는 많은 응용 분야에서 정제과정 없이 사용되었다. 그러나 페놀성 하이드록시기에 대한 화학적 개질 반응을 수행하면 성능이 향상될 수 있다. 리그노술포네이트의 설포네이트 그룹의 존재는 수성 시스템에서의 적용을 용이하게 한다. 이 경우, 활엽수 기반 리그노술포네이트보다 메톡시 그룹이 적기 때문에, 침엽수 기반 리그노술포네이트가 바람직할 수 있다. 시판되는 리그노술포네이트는 불순물을 많이 함유하기 때문에 수정에 적합한 특성을 가진 리그노술포네이트를 얻기 위해서는 추가적인 정제 단계가 필요하다. 그러나 이 단계는 리그노술포네이트 개질 비용을 증가시킨다. 더욱이, 리그노술포네이트의 생산량과 그에 따른 가용성이 세계적으로 감소하고 있어 사용 가능한 리그노술포네이트 기반 제품이 감소하고 있다.
2.4 유기용매 리그닌(Organosolv lignin)
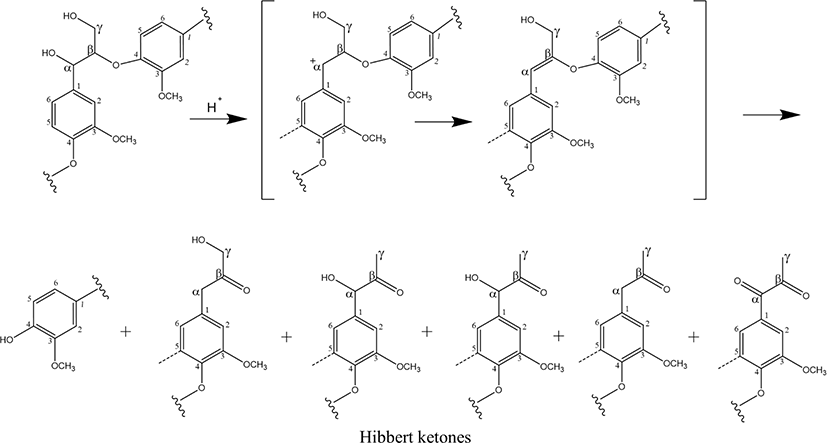
유기용매 리그닌의 추출은 바이오 에탄올을 생산할 때 쓰이는 방법으로, 추출 방법은 크게 두 가지가 있다. 포름산이나 아세트산과 같은 산 유기용매를 이용하는 조건과 메탄올이나 에탄올 같은 알코올 용매를 이용하는 방법으로, 약 140~200°C의 온도 조건하에서 추출하게 된다. 펄프화 과정에서 불안정한 β-O-4 결합은 일반적으로 산성 가수분해 경로를 통해 끊어져 케톤기가 만들어진다(Figure 5).15,21 리그닌의 극성, 구조 및 특징은 사용된 용매에 따라 서로 다른 특성을 갖는다. 이 방법은 40~60 wt.% 물과 에탄올 혼합물로 추출되며, 추출된 리그닌은 묽은 알카리 용액과 물, 에탄올 혼합물에 용해된다. 용해된 리그닌은 농축한 후, 물에 침전시켜 회수하게 된다. 생성된 리그닌은 고운 갈색의 자유 유동 분말로, 일부 유기용매 및 희석 알칼리 수용액에 용해된다. 유기용매 리그닌은 중성 또는 산성 pH에서 물에 녹지 않는다. 또한, 그들은 수 평균 분자량이 1,000 미만이고 다분산도가 2.4~6.3 사이 값을 가진다. 유기용매 리그닌은 천연 리그닌과 유사하게 황 원소가 없고, 회분 함량이 낮으며 소수성이 더 높은 경향이 있다. 또한, 다분산도와 유리전이온도가 낮다.43
유기용매 리그닌과 크래프트 리그닌을 비교해보면, 비슷한 탈 리그닌 처리과정에서 두 리그닌 유형에 풍부한 β-에테르 결합이 유사하다고 보고되었다.45 유기용매 리그닌은 난연제, 농약용 서방제, 계면활성제, 산화방지제, 아스팔트 증량제, 리그닌 유래 화학 물질의 원료 공급원 등으로 사용된다.46 그러나 유기용매 리그닌 추출 공정의 주요 단점은 용매 회수 비용이 높고, 용매의 열적 불안정성과 용매 사용으로 인해 공정 폐수가 발생한다.27,47 공정상에 용매를 사용하면 공정 시스템이 복잡해지고(고압 용기의 필요성 대두) 용매 회수율이 떨어진다. 또한, 이 과정에서 용매를 사용하면 미생물의 발효와 효소 가수 분해에 대한 억제 효과가 있는 것으로 보고되었다.48,49 유기용매 리그닌은 소수성이며, 유기 용매에 상대적으로 잘 용해된다.
유기용매 리그닌은 아황산염 및 크래프트 리그닌보다 더 높은 품질과 순도를 가지고 있지만, 생산단가가 상대적으로 더 높다. 유기용매 리그닌은 약 1.7%의 회분, 1.0~3.0%의 당, 7.5%의 수분을 포함하지만 황 원소는 포함하지 않는다.20 더욱이, 유기용매 리그닌은 다른 리그닌 유형(즉, 크래프트 또는 리그노술포네이트)과 비교할 때 가장 낮은 분자량(< 5,000 g/mol)을 갖고 있다. 황 원소 함유 리그닌을 활용하는 응용 분야 이외에도, 무황 리그닌은 특히 폴리우레탄 폼, 목재 패널 및 에폭시 수지 생산 공정과 같이 냄새 방출이 우려되는 공정에 적용할 수 있다.38,46 한편, 일부 응용 분야는 저 분자량 또는 고분자량의 특정 분자량의 리그닌이 요구되며, 유기용매 리그닌은 다른 유형의 리그닌보다 분자량이 낮기 때문에 더 나은 역할을 할 수 있다. 이 기능은 특정 용매에서 리그닌의 용해도를 높이고 잉크, 페인트 및 바니시의 필러와 같은 일부 공정에서 리그닌의 사용을 용이하게 할 수 있다.50 그럼에도 불구하고, 유기용매 리그닌의 저분자량은 결합제 및 접착제와 같은 응용 분야에서의 사용을 저해할 수도 있다.20
유기용매 리그닌은 무황 성분으로 인해 동물 사료의 영양으로 주로 사용되었다.27 이 리그닌을 생산하기 위해 활엽수 목재 원료가 주로 사용되었으며, 이로 인해 유기용매 리그닌의 수용성이 낮아지게 된다. 유기용매 리그닌은 수지, 목재 접착제, 가소제, 난연제 및 흡착제 및 분산제와 같은 일부 수용성 제품과 같은 대부분의 불용성 제품을 생산하기 위한 원료로 사용되었다. 유기용매 리그닌은 천연 리그닌에 가까운 구조를 가지고 있지만, 이 리그닌의 상업적 생산 능력이 더 작기 때문에 크라프트 리그닌에 비해 활용도가 낮다. 결론적으로, 고순도 유기용매 리그닌은 페놀 수지와 같이 고순도를 요구하는 응용 분야에 사용될 수 있다.
2.5 증기폭쇄 리그닌(Steam explosion lignin)
증기 폭쇄 공정은 19세기 초에 개발된 공정이다. 짧은 시간 동안 약 200°C 이상의 고압 증기로 고압(약 3.5 MPa)하에서 1~20분 동안 노출시켜 수행된다.51 이 과정은 리그닌과 헤미셀룰로오스 사이의 결합을 끊을 뿐만 아니라 헤미셀룰로오스와 일부 셀룰로오스 사이의 결합도 분해를 일으킬 수 있다.21 이는 바이오 매스의 화학 구조를 파괴하고, 유기산을 형성하여 글리코사이드의 가수분해를 유도하여 β-O-4 함량이 감소한다. 증기 폭쇄 처리 후, 리그닌의 약 90% 정도가 알카리 또는 유기용매 추출로 리그닌을 회수할 수 있다.38 이 공정으로 얻어진 증기 폭쇄 리그닌은 유기용매 리그닌보다 저분자량을 가지며 크래프트 리그닌에 비해 유기용매 용해성이 상대적으로 높다. 또한, 리그닌 구조는 페놀성 방향족이 3~12개 정도의 올리고머로 구성되어 있는 것으로 보고되고 있다.46
리그닌의 최근 활용 동향
리그닌은 새로운 고부가가치의 화학 물질 전구체로 평가되고 있으며, 생분해가 가능하고, 항산화제나 안정제로 사용될 수 있기 때문에 최근 매우 각광 받고 있는 재료이다. 대부분의 활용기술은 고분자인 리그닌을 분해하는 수소분해, 열분해, 산화, 가수분해 등이 있고, 활성 관능기를 이용한 화학적 개질은 알킬화, 아민화, 설폰화 등이 있다. 또한, 하이드록시기에 기능화를 부여하기 위해 페놀화, 우레탄화, 에테르화 반응을 통하여 그래프팅할 수도 있다.52
최근에는 에너지 저장장치, 약물 전달, 나노 복합재, 여과장치 등으로 다양한 연구 개발을 수행하고 있다. 이러한 리그닌은 다분산성을 띄는 구조를 형성하고, 폴리페놀 구조에 페놀성 하이드록시기가 존재하기 때문에 선택적 메틸화에 의해 라디칼을 제거하며, 이는 열안정성에도 기여한다.53 대부분 상업적으로 응용되는 리그닌은 리그노술포네이트이다. 리그노술페이트는 주로 분산제로 사용되고, 콘크리트 혼합물에 적용될 수 있으며, 동물사료의 펠렛 내구성과 내마모성을 개선하고, 압출기의 마모를 줄이기 위해 사용된다. 리그닌의 많은 방향족 그룹은 탄화하기 좋은 전구체가 될 수 있으며, 탄화된 리그닌은 촉매 및 에너지원 뿐만 아니라 카본블랙(carbon black) 충진재의 대체재로 사용될 수 있다.20,54,55 바이오 디젤을 만들기 위해 리그닌 유래 촉매를 제작하면 촉매 활성이 크고, 전기방사를 통해 탄소 매트를 제작할 수도 있다.56
1. 난연제(fire retardants)와 산화방지제(antioxidants)
화재로부터 안전한 사회를 위한 화재예방에 대한 요구가 지속적으로 대두되고 있으며 이를 충족시키기 위해 난연제 제조에도 지속 가능한 천연 소재의 적용이 활발히 연구되고 있다. 합성 화합물 대신, 최근 연구에서는 리그닌이 천연 난연제로 사용될 수 있으며,57 난연성 고분자 시스템에 적용하려는 움직임이 있다.
리그닌은 PP, PBS, ABS, PET와 같은 범용 고분자의 가연성을 효과적으로 감소시킬 수 있다는 것이 보고되었다.58 리그닌을 함유한 합성 고분자 및 생체 고분자는 고분자 단독 대비 낮은 가연성을 유지하고, 연기 방출을 감소시켰다. 리그닌 내에 메톡시 그룹과 하이드록시기의 존재로 인한 리그닌의 복잡한 방향족 특성은 항산화 역할을 유도한다. 이러한 작용기는 자유 라디칼 제거 활동을 통해 산화반응을 종결시킨다. 나노크기의 리그닌 입자는 벌크 리그닌보다 더 우수한 항산화 및 UV 보호 특성을 갖는 것으로 보고되었다.59 이러한 특성의 리그닌 나노 입자는 화장품, 제약 및 식품 산업에 적용될 것으로 예상된다.
2. 에너지원(energy source)
리그닌을 탄화시킴으로서 열과 전기를 얻는데 사용될 수 있으며, 건조된 리그닌의 평균 열량은 약 25 MJ/kg이다. 일반적으로 석탄의 에너지 밀도는 24~30 MJ/kg으로 리그닌은 석탄 에너지와 비슷한 역할을 수행할 수 있다.60 석탄과 리그닌을 동시에 사용하면 흑탄만 사용하는 보일러에 비해 보일러 효율이 38% 증가하고, 탄소 배출량이 약 60% 정도 감소시킬 수 있다. 또한, 리그닌을 열 분해하게 되면 바이오 오일, 바이오 숯, 가스화가 가능하며, 공정 조건과 공급 원료, 반응속도나 첨가제에 따라 달라질 수 있다.
일반적으로 낮은 온도와 가열 속도에서 숯이 생성되고, 높은 가열 속도와 체류시간에서 리그닌은 액화된다. 높은 온도, 긴 체류시간, 느린 가열속도는 합성가스(syngas)를 만들기에 적합하다. 바이오 오일은 낮은 발열량, 불완전한 휘발성, 산도 등으로 인해 사용하기엔 많은 제약이 존재하며 가스화를 하게 되면 고부가가치 에너지원이 될 수 있다.61 합성가스는 일산화탄소, 이산화탄소, 수소 등으로 구성되어 있고, 공정뿐만 아니라 난방 및 전기생산에도 사용될 수 있는 장점이 있다.
3. 에너지 저장장치 소재(energy storage)
에너지 저장장치에 리그닌을 적용하는 것은 비용 절감이 가능하고, 친환경적인 측면에서 유리하다. 리그노술포네이트 (lignosulfonate; LS) 가 납축 전지의 음극 페이스트에 대한 확장제로 사용될 수 있다는 것이 보고되었다.62 충전과 방전 사이클을 통해 사이클 수명, 균열 능력, 효율 극대화, 내구성을 높이는 것으로 보고되었다. 리튬 1차 전지는 무기화합물 기반 음극과 전해질을 포함하며 재생이 불가능하고, 독성이 있으며 비싸다는 단점이 있다.63
리튬 이온 배터리의 제조시간과 비용을 절감하기 위해 리그닌을 원료로 사용한 탄소 나노 섬유와 탄소 섬유 매트가 적용된 경우가 있다.64 또한, 리그닌의 재생가능한 이점 때문에 리그닌에서 파생된 활성탄은 초전도체를 만드는데 쓰일 수 있다. 태양 전지의 경우, 리그닌을 연료 감응형 태양전지와 고분자 전지를 대체할 수 있는 감광제를 개발하는데 사용되고 있다.65
4. 시멘트(cements)
건설현장에서 사용되는 시멘트를 효율적으로 사용하기 위해 리그닌을 함유한 시멘트에 대한 연구가 진행되고 있다.66-68 리그닌 또는 개질된 리그닌을 시멘트에 혼합할 경우 높은 성능을 가진 콘크리트를 형성할 수 있는 것으로 알려져 있다. 높은 강도를 지니고, 연삭을 용이하게 하며 습기 및 산성비로 인한 외벽 손상을 줄일 수 있다. 또한, 리그닌은 시멘트 페이스트의 압축 강도를 향상시킬 수 있다. 설폰화 공정은 리그닌에 황산염을 투입시켜 리그닌의 높은 제타 전위로 인해 시멘트 매트릭스에서 분산제처럼 작용하도록 하는데, 이와 같은 높은 전하가 시멘트 입자 사이에 정전기 반발을 일으키는 원리이다.69
5. 바인더(binders)
수용성 리그닌 염은 수성 안료 인쇄 조성물에서 결합제로 사용하기에 적합하다.70 리그노술포네이트의 저비용 바인더는 일반적으로 성형탄(coal briquettes) 또는 세라믹, 광물분진탄(briquetting of mineral dust; 미세분말, 부스러기 등) 및 합판, 파티클 보드와 같은 목재 관련 재료에도 사용될 수 있다.71 리그닌을 결합제로 사용하기 위해서는 반응성을 향상시켜야 하는데, 이는 페놀화나 에폭시화, 탈메틸화 등의 화학적 개질을 수행할 수 있다. 또한, 에폭시 수지나 페놀 수지 등에 직접적으로 리그닌을 개질시키거나 직접 컴파운딩 할 수 있다.72
6. 나노소재(nanomaterials)
최근 나노 과학 기술은 재료 구조, 특성 및 성능 향상에 주목하고 있다. 고가 재료를 설계하기 위한 나노 규모의 리그닌은 아직 초기 단계에 있다. 리그닌의 복잡하고 거대한 분자 구조를 나노 입자, 나노 튜브 및 나노 섬유로 제작하는 것이 가능하다. 이 방법은 리그닌을 보다 균일한 크기와 모양으로 만드는데 도움이 된다.73
나노 입자의 높은 표면적 대 부피 비율은 고분자 매트릭스를 강화하고, 항산화 특성을 통해 열 안정성을 향상시킬 수 있다. 리그닌 나노 입자는 소수성 매트릭스에서 우수한 분산성과 혼화성을 나타낸다. 리그닌 나노 입자의 작용기는 고부가가치 응용 분야를 위해 설계될 수 있다. 계면간 가교, 중합, 용매 교환 및 초음파 처리와 같은 처리 방법이 리그닌 나노 입자의 모양과 크기에 영향을 미치는 것으로 보고되었다.74 하이드로젤 (hydrogel) 기술의 발전은 바이오 기반 특성, 생체 적합성, 생분해성, 효소 분해 및 생태학적으로 안전한 특성을 지니며, 나노 크기의 리그닌에 대한 많은 관심을 받고 있다. 약물 전달, 상처 관리, 조직 공학 및 콘택트 렌즈에서 리그닌 기반 하이드로젤이 평가되고 있다.75
7. 생체의용 소재(biomedical materials)
리그닌 유래 하이드로젤은 줄기세포, 암 연구, 세포 치료, 조직 공학, 면역 조절 및 체외 진단에 사용될 수 있다. 또한, 리그닌은 보호 역할을 수행할 수 있으며, 리그노술포네이트는 산화 활동을 감소시켜 면역 체계를 자극하는 약물을 개발하는데 투입될 수 있다. 잔탄검(xanthan gum)과 리그닌은 향상된 열 산화 특성과 항균 활성으로 생분해성 하이드로젤로 적용 가능하다는 사실이 입증되었다.75,76 약물 전달, 상처 케어, 조직 공학 및 콘택트 렌즈에서 리그닌 기반 하이드로젤이 평가되고 있다.77
8. 하이드로젤(hydrogels)
하이드로젤은 물리, 화학적으로 가교된 3차원 친수성 네트워크로서 물이나 수용액에서 팽창한다. 우수한 생체 적합성, 조직 모방 능력, 높은 수분 흡습성 등의 특성을 갖고 있어 바이오센서나 약물 전달 등의 분야에 적합하다. 리그닌은 생체 적합성, 생분해성, 낮은 독성 등의 고유한 특성을 가지고 있기 때문에 하이드로젤 분야에서 다양한 연구가 진행되고 있다.78,79
초기 연구에는 acrylamide와 polyvinylalcohol (PVA)을 크래프트 리그닌과 copolymer로 제조하고, acrylamide 단량체와 혼합하여 리그닌 하이드로젤을 제조하였다. 크래프트 리그닌은 알카리성 리그닌 하이드로젤과 달리 높은 팽윤비와 팽창 속도, 느린 물 흡수 특성을 보여주었는데, 이는 리그닌의 네트워크 구조에 따라 다른 특성을 보인다는 것을 나타내었다.80 Polyethylene glycol glycidyl ether는 기계적 안정성을 나타내는 팽윤 특성을 보였으며, 리그닌의 가교제로 사용되었다. 리그닌과 PEGMA/cyclodextrin를 이용하여 원자 이동 라디컬 중합(atom transfer radical polymerization; ATRP)에 의해 하이드로젤을 제조하였는데, 우수한 유변학적 특성과 높은 자가 치유능력, 기계적 반응성이 우수하였다.81
9. 금속이온 봉쇄제(sequestering agents)
중금속 오염은 금속 도금, 채광 작업, 제혁소, 제련 및 합금 공장, 축전지 산업과 같은 다양한 산업에서 발생하는 폐기물의 방출로 인해 발생한다. 활성탄은 중금속을 흡착하기 위해 가장 널리 사용되는 재료지만 활성탄 사용은 비싸다는 단점이 있다.82 Pb, Hg, Cd, Cr, As, Zn, Cu 및 Ni와 같은 독성 중금속 이온을 효율적으로 제거하기 위한 연구가 진행되고 있다. 연구자들은 리그닌 구조의 변형이 중금속을 제거하는 흡수 능력을 향상시킬 수 있음을 입증하였다.83
리그노술포네이트는 금속 이온을 포집하고, 착물을 형성하는 강력한 격리제로 보고된 바 있다.84,85 리그노술포네이트는 토양 개선, 토양 조절 또는 유해 금속 제거에 적용될 수 있다. 또한, 리그닌은 제초제, 살충제 및 비료의 제어 방출제로 평가되고 있다.86 게다가, 리그닌 하이드로젤은 농업 및 임업에서 물 저장 토양 조절제로 성능 테스트가 수행 되었다. 초흡수 능력을 가진 lignosulfonate-g-acryl acid 하이드로젤은 폐수에서 오염물 흡수 및 염료(메틸렌 블루) 제거 가능성을 보여 주었다.87 살충제에 리그닌을 첨가하면 광분해에 대한 안정성이 향상되는 것으로 보고되고 있다.88
리그닌 기반 고분자 복합소재 활용 동향
고분자 블렌드는 상호 확산을 통해 상호 작용하는 두 개 이상의 혼합물이며, 복합재에서 중합체와 강화제는 계면에서 흡착을 통해 물리적 상호 작용한다. 상호 확산의 정도는 구성 요소의 상호 작용에 따라서 계면결합 정도가 달라진다. 약한 상호 작용은 큰 분산입자와 이질적인 혼합을 초래하는 반면, 강한 상호 작용은 관찰 가능한 입자가 없는 균일한 계면을 형성한다.89-91 따라서 상호 작용은 이종 블렌드에서 상호 용해도와 계면 접착 강도를 결정하게 된다. 리그닌은 복합재의 필러로 첨가되고 있으며, 다양한 바이오 재료로써 사용되고 있다. 하지만 리그닌은 수많은 극성관능기를 갖고 있기 때문에 자가 상호 작용이 강해 고분자 블렌드 시, 매트릭스와의 상호 작용 및 혼화성을 증진시킬 수 있어야 한다. 또한, 매트릭스와 접촉하는 면적이 넓을수록 종횡비가 높아져 인장강도가 개선되고, 유연성이 있어야 한다.92
이를 위해 필러로 첨가되는 리그닌의 입자크기를 작게 만들어 매트릭스와 리그닌입자 사이에 공간(voids) 형성을 감소시키고, 리그닌 표면에 존재하는 하이드록시 기를 개질하여 분산성을 향상시키거나, 복합재와 필러 사이 상용성을 부여하기 위해 상용화제를 첨가하기도 한다. 리그닌의 활성도를 높이기 위해 반응성 관능기인 하이드록시기를 phenolation, oxypropylation, esterification 등의 화학적 개질을 통하여 리그닌 그래프트 공중합체를 만든다.93-95 그래프트 된 리그닌은 “grafting from” 및 “grafting to”의 두 가지의 접근법으로 분류할 수 있다. 그 중에서도 “grafting from”이 주로 선호되며, 개환 중합(ring-opening polymerization)과 같이 링 형태 단량체의 고리가 열리면서 리그닌 내 하이드록시기와 반응하여 단량체의 사슬이 리그닌 표면에 고분자로 성장한다. 가장 자주 쓰이는 단량체는 락타이드(lactide)나 카프로락톤(caprolactone) 등이 사용된다.96 화학적 개질 반응은 리그닌을 더 가치있게 만들고, 다양한 재료로 접목할 수 있게 만드는 방법이다.
일반적으로 리그닌의 녹는점은 140~170°C의 범위를 가지며, 열가소성 폴리머 매트릭스내 충진재로 적합하다.97,98 많은 양의 필러를 고분자 매트릭스에 첨가하는 것은 상당히 어려우며, 리그닌이 최대 40 wt.% 첨가되면 매트릭스와 호환성이 떨어지지만, 화학적 개질을 통한 리그닌 유도체는 고충진 가능성을 보여준다. 이는 리그닌 일부가 반응에 참여하지 않고, 충진제 역할을 하여 불규칙한 네트워크 구조를 유발하기 때문에 기계적 특성이 저하되게 된다. 하지만, 크래프트 리그닌을 사용하면 충진 함량을 최대 80 wt.%까지 첨가할 수 있어, 매트릭스의 인장강도와 탄성율을 크게 향상시킬 수 있다.99 다양한 리그닌 충진제는 고성능 특성을 나타내며, 리그닌의 첨가로 결정성 고분자인 경우에 결정화 속도와 결정화도를 향상시킬 수 있고, 열적 특성을 개선할 수 있다. 대부분의 연구에서는 열경화성 수지에 리그닌을 첨가하며, 주로 phenol-formaldehyde (PF), polyurethane (PU), epoxy (EP) 등이 있다.100,101
1. 페놀 수지(phenol resin)
목재용 접착제는 포름알데하이드나 페놀, 요소, 에폭시 등의 수지를 적용하고, 인장강도가 높지만 발암물질을 포함하기 때문에 독성이 있다. 폴리 페놀 구조와 유사성을 지닌 리그닌을 첨가하게 되면 그만큼의 독성을 줄일 수 있어 대체 가능한 목재 접착제를 적용할 수 있다.102 낮은 유리전이온도, 낮은 다분산성, 높은 소수성과 같은 특징으로 인해 합판 또는 패널 접착제로 사용하기 적합하지만 화학적 이질성은 고분자 레진에 많은 제약이 따른다. 따라서 리그노술포네이트, 크라프트 리그닌, 유기용매 리그닌, 소다 리그닌 등이 더 많은 고리 위치, 더 높은 분자량 및 높은 열분해 온도 때문에 페놀 대체 물질로 유망하다.103
2. 에폭시 수지(epoxy resin)
에폭시 수지는 amine, anhydride, carboxylic acid 및 hydroxy group 형태의 반응성 수소 원자를 포함하는 경화제와 가교될 수 있으며, 리그닌은 carboxylic acid 및 hydroxy group 모두 함유되어 있기 때문에 화학적 개질 없이 직접 적합한 경화제가 될 수 있다. 리그닌 표면을 에폭시 링으로 개질하여 에폭시화 하거나 리그닌을 에폭시 수지의 경화제로 적용될 수 있다. 에폭시 고리 치환의 경우, 알카리 분위기를 형성하여 리그닌의 하이드록시기와 epichlorohyrine을 반응시켜 옥시란 (oxirane) 고리를 형성시킨다. 이렇게 형성된 에폭시 복합재의 열 안정성은 석유유래 기반 에폭시보다 떨어지지만 저항성 시험(250~280°C)을 통과할 정도의 특성을 보여주었다.104,105
3. 폴리우레탄 수지(polyurethanes)
폴리우레탄은 중량 대비 강도, 에너지 흡수 성능 및 단열 특성 덕분에 자동차, 포장 산업 등에서 주로 사용되는 소재이다. 기존 폴리우레탄은 친환경적이 아닌 화학적 합성에 의해 만들어지는데, 이소시아네이트(isocyanate)와 폴리올(polyol)과 같은 다가 알코올의 하이드록시기가 반응하면서 합성되며, 리그닌의 하이드록시기가 폴리올을 대체할 수 있다. 리그닌 기반 폴리우레탄 폼의 특성은 기존 폴리우레탄보다 우수하거나 비슷한 것으로 알려져 있다.106 리그닌 기반 폴리우레탄 발포체에 대한 VOCs (volatile organic compounds) 저감연구107와 그들의 점탄성 거동은 함유된 리그닌이 폴리우레탄의 가교 효과를 제한하고 충진제 역할을 하여, 경질 세그먼트에 크게 의존한다 연구가 보고되었다.108
4. 폴리올레핀 수지(polyolefins)
폴리올레핀은 크게 polyethylene과 polypropylene으로 나눠지며, 극성기가 없어 강한 소수성을 지닌 고분자이다. 따라서 다른 고분자와 혼합되기 어렵다고 알려져 있으나, 리그닌과 블렌딩될 경우, 리그닌의 페놀성 하이드록시기가 고분자의 자유 라디칼을 억제할 수 있기 때문에 안정제의 역할을 할 수 있으며, 고분자 매트릭스의 항산화가 가능하다.109 페놀성 하이드록시기는 라디칼을 억제하여 안정성에 기여할 수 있지만, 매우 높은 당량비로 인해 기존 저분자량 안정제보다 효율성이 떨어진다. 고분자에 첨가되는 리그닌의 함량이 높아질수록 균일한 분산성과 혼화성을 향상시켜 기계적 물성 개선이 중요하게 작용한다. 리그닌과 블렌딩한 결과, 다양한 특성에서 여러가지 연구 결과가 관찰되었다. 리그닌 분자의 강한 극성때문에 모듈러스는 일반적으로 증가하지만 강도와 변형성은 종종 저하된다.110-114 리그닌과 폴리올레핀의 약한 상호 작용 때문에 리그닌을 화학적으로 다양하게 개질하거나 커플링제를 물리적으로 혼합하여 사용해야 한다는 것이 입증되었다.115
5. 폴리하이드록시 알카노에이트 [poly(hydroxy alkanoate)]
폴리하이드록시 알카노에이트 [poly(hydroxy alkanoate); PHA]는 생분해 기반 분해성 고분자로서 지방족 폴리에스터 종류중 하나이다. 주로 박테리아나 곰팡이 균주에 의해 합성되며, 물에 용해되지 않는다. 또한, O2, CO2, H2O에 투과도가 낮기 때문에 PHA는 필름, 코팅, 봉지재 등에 적용된다.116 PHA 계열로 가장 널리 사용되는 고분자는 PHB [poly(hydroxybutyrate)]이다. PHB에 리그닌을 사용하게 되면 리그닌의 페놀성 하이드록시기로 인해 혼화성이 향상되지만, 인장강도와 열안정성은 감소한다. 40 wt.%의 리그닌을 함유한 PHB의 DSC 결과에서 단독 유리전이온도를 보여주었다.117 유변학적 결과에서, 리그닌 함량이 30 wt.% 미만일 때, PHB의 가소제로 작용함을 보여주었다. 또한, 리그닌 함량이 60 wt.%일 때 PHB 매트릭스와 상분리가 일어나 복합재의 점도가 증가하고, 에너지가 감소하였다. 리그닌이 첨가된 다양한 복합재들은 내수성, 인장강도, 열 안정성을 향상시켰지만, PHB 복합재에서는 낮은 인장강도와 열 안정성을 보여주었다. 이는 바이오 고분자의 다양한 구조와 관련이 있다.118 바이오 고분자에 리그닌 첨가량은 최대 30 wt.%이며, 리그닌 복합재가 바이오 고분자를 대체할 때, 잠재적인 대체 고분자가 될 것이다.
6. 폴리유산 [poly(lactic acid)]
폴리 유산 [poly(lactic acid); PLA]은 자연계에서 쉽게 분해되는 생분해성 고분자로, 다양한 산업에 가장 널리 사용되고 있다. 하지만 PLA는 취성이 매우 강하고, 높은 생산 비용으로 인해 단가가 높고, 열악한 열안정성 등의 단점이 존재하기 때문에 개질한 리그닌을 통해 물성을 향상시켜왔다. 셀룰라아제 효소처리 리그닌(cellulase enzyme lignin; CEL)/폴리올레핀 그래프팅 말레산 무수물(polyolefin-g-maleic anhydride)/PLA 블렌딩에서 CEL이 상용화제 역할을 하여 혼화성을 증가시킨다고 보고되었다.67 PLA는 lactide의 축합 중합과 개환 중합을 통해 합성될 수 있으며, 축합 중합은 물을 제거하는데 어려움이 있어, 대부분 개환 중합을 통해 고분자로 만들어진다.
7. 고무(Rubber)
리그닌과 고무 매트릭스 사이의 계면 결합 강도를 높이는 방법으로 화학적 개질법이 널리 알려져 있다. 이는 리그닌 입자의 고무 매트릭스 간 분산력뿐 만 아니라, 계면접착력이 떨어지져서 고무 매트릭스 내에서 리그닌 입자의 강화 효과가 카본 블랙을 사용했을 때 만큼 좋지 않기 때문이다. 고무 기반 응용 분야의 화학적 개질 전략은 일반적으로119 리그닌 표면의 화학적 개질,120 리그닌과 고무 매트릭스 사이 화학적 연결을 형성할 수 있는 작용기를 포함하는 대체 화학물질 또는 첨가제를 이용할 수 있다.
많은 연구자들은 리그닌과 고무 매트릭스 간 강화 효과를119-123 향상시키기 위해 다양한 연구방법을 시도하고 있으며, 이를 통해 많은 성능개선의 가능성을 확인하였다.124,125 고무-리그닌 계면 결합을 개선하기 위해 커플링제 및 접착제를 사용하는 기술도 보고되었다.126,127 이러한 접근법은 리그닌과 고무 매트릭스 사이에 공유 결합을 생성하여 계면 결합을 향상시켰으며, 화학적 개질은 헥사메틸렌테트라민(hexamethylenetetramine)125,128-130 및 사이클로헥실아민(cyclohexylamine)134을 사용한 리그닌의 표면 개질을 통해 리그닌 충진제와 비극성 고무 매트릭스 사이의 상용성을 개선을 도모하였다. 이러한 처리 방법은 기본적으로 리그닌과 포름알데히드의 반응을 수반하며, 우수한 내마모성과 타이어 물성 향상을 제공하는 것으로 보고되고 있다. 고무 매트릭스에서 리그닌의 분산 및 상용성을 향상시키기 위한 최근의 새로운 접근 방식으로 이중 가교 네트워크의 구성을 도입하는 방법이 제안되었다.
이중 가교 네트워크는 고무의 황 원소와 탄소 원자 사이에 형성된 공유 결합과 리그닌과 Zn2+ 이온 사이에 형성된 비공유 결합으로 구성되어 있다. 고성능 리그닌 함유 고무의 개발은 Zn 기반 배위 결합130을 만들고 황 원소 공유 결합과 희생 결합(sacrificial bond)의 동적 배위로 구성된 네트워크를 형성하여 연구되고 있다. 이러한 결합의 매커니즘은 강하고 질긴 고무 화합물의 뛰어난 특성을 제공할 수 있다.132-135 또한, 나노 리그닌을 콜로이드성 리그닌-폴리(디알릴디메틸암모늄 클로라이드)(PDADMAC)로 개질하여 복합체(LPC)로 컴파운딩을 진핼할 때, 천연고무/리그닌 나노복합체는 높은 기계적 물성향상을 보여주었다.136 리그닌은 페놀성 하이드록시기와 카르복실기가 이온화될 때 음이온성 고분자 전해질(colloid)로 간주되었다. 결과적으로 LPC는 천연고무(natural rubber; NR) 매트릭스에 균일하게 분포되어 NR/LPC 복합재의 기계적 특성과 열 및 열산화 안정성이 향상시켰다. 또한, 하이드록시기의 아세틸화와 같은 화학적 개질도 고무 매트릭스에서 상용성 및 분산성 측면에서 동일한 개선효과를 달성하는 것으로 보고되었다.137,138
Conclusion
화학적으로 복잡한 구조를 지닌 리그닌은 적절한 규격화가 어렵고, 사용되는 추출기술에 의해 그들의 화학구조가 크게 의존한다. 리그닌은 표면에 더 많은 반응 부위를 제공하는 페놀 하이드록시기와 침엽수 기반 리그닌의 메톡시 그룹이 적을수록 페놀 하이드록시기에 대한 입체 장애가 줄어들고 수용성이 높아진다. 다양한 형태의 리그닌의 특성을 파악하고, 적절한 적용 기술들을 개발하는 것이 친환경 소재로서의 리그닌 활용도를 극대화할 수 있다. 특히, 리그닌은 수많은 극성그룹으로 인해 자가 상호작용이 매우 강하기 때문에, 이 상호작용에 따라 일반 고분자 매트릭스와의 계면 결합력이 결정된다. 따라서, 리그닌 표면을 개질하거나 가소화 및 커플링제를 사용하여 고분자 매트릭스 내에서 분산력을 향상시켜야 한다. 리그닌은 다양한 고분자 내에 반응성 재료로 작용할 수 있어, 리그닌의 형태와 구조의 제어 및 화학적 변형을 통해 리그닌의 기능화에 대한 연구 개발이 필요하다. 향후, 리그닌의 연구 방향은 고분자 복합소재의 충진재뿐만 아니라 에너지 저장, 열전 장치, 바이오 센서, 제어 약물 전달, 유전자 치료, 치료 시스템 과 같은 첨단 응용을 위한 나노 구조 소재 개발도 함께 진행되어야 할 것이다.
Acknowledgments
이 논문은 2021년도 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 기초연구사업(No. 2021R1F1A104965211)과 경기도 지역협력 연구사업(GRRC 단국 2016-B01)에 의해 지원되었으며 이에 감사드립니다.
References
F. Sarasini, J. Tirillò, D. Puglia, F. Dominici, C. Santulli, K. Boimau, T. Valente, and L. Torre, “Biodegradable polycaprolactone-based composites reinforced with ramie and borassus fibres”,
Compos. Struct.,
167, 20 (2017).


M. A. Huneault and H. Li, “Morphology and properties of compatibilized polylactide/thermoplastic starch blends”,
Polymer,
48, 270 (2007).


M. Brodin, M. Vallejos, M. T. Opedal, M. C. Area, and G. Chinga-Carrasco, “Lignocellulosics as sustainable resources for production of bioplastics - A review”,
J. Clean. Prod.,
162, 646 (2017).


C. K. Yong, Y. C. Ching, C. H. Chuah, and N.-S. Liou, “Effect of fiber orientation on mechanical properties of kenaf-reinforced polymer composite”,
Bioresources,
10, 2597 (2015).


X. Zhou, F. Zheng, C. Lv, L. Tang, K. Wei, X. Liu, G. Du, Q. Yong, and G. Xue, “Properties of formaldehyde-free environmentally friendly lignocellulosic compositesmade from poplar fibres and oxygen-plasma-treated enzymatic hydrolysis lignin”,
Compos. Part B Eng.,
53, 369 (2013).


V. Hemmilä, J. Trischler, and D. Sandberg, “
Lignin : an adhesive raw material of the future or waste of research energy?”, In Proceedings of 9th Meeting of the Northern European Network for Wood Science and Engineering (WSE)”, Eds. by C. Brischke, and L. Meyer, 98 (2013).

M. F. Rosa, B. Chiou, E. S. Medeiros, D. F. Wood, T. G. Williams, L. H. C. Mattoso, W. J. Orts, and S. H. Imam, “Effect of fiber treatments on tensile and thermal properties of starch/ethylene vinyl alcohol copolymers/coir biocomposites”,
Bioresour. Technol.,
100, 5196 (2009).



N. Graupner, “Application of lignin as natural adhesion promoter in cotton fibre-reinforced poly(lactic acid) (PLA) composites”,
J. Mater. Sci.,
43, 5222 (2008).


I. Spiridon, K. Leluk, A. M. Resmerita, and R. N. Darie, “Evaluation of PLA–lignin bioplastics properties before and after accelerated weathering”,
Compos. Part B Eng.,
69, 342 (2015).


S. S. Nair, H. Chen, Y. Peng, Y. Huang, and N. Yan, “Polylactic acid biocomposites reinforced with nanocellulose fibrils with high lignin content for improved mechanical, thermal, and barrier properties”,
ACS Sustainable Chem. Eng.,
6, 10058 (2018).


A. Duval and M. Lawoko, “A review on lignin-based polymeric, micro- and nano-structured materials”,
React. Funct. Polym.,
85, 78 (2014).


C. Pouteau, P. Dole, B. Cathala, L. Averous, and N. Boquillon, “Antioxidant properties of lignin in polypropylene”,
Polym. Degrad. Stab.,
81, 9 (2003).


K. Sahakaro, N. Naskar, R. N. Datta, and J. W. M. Noordermeer, “Blending of NR/BR/EPDM by reactive processing for tire sidewall applications. I. Preparation, cure characteristics and mechanical properties”,
J. Appl. Polym. Sci.,
103, 2538 (2006).


N. G. Lewis and E. Yamamoto, “Lignin: occurrence, biogenesis and biodegradation”,
Annu. Rev. Plant Physiol. Plant Mol. Biol.,
41, 455 (1990).



G. Henriksson, “
Lignin”, In “
Wood chemistry and wood biotechnology”, Eds. by M. Ek, G. Gellerstedt, and G. Henriksson, Walter de Gruyter, 121 (2009).

A. Holmgren, G. Brunow, G. Henriksson, L. Zhang, and J. Ralph, “Non-enzymatic reduction of quinone methides during oxidative coupling of monolignols: implications for the origin of benzyl structures in lignins”,
Org. Biomol. Chem.,
4, 3456 (2006).



W. G. Glasser, “
Classification of lignin according to chemical and molecular structure”, In “
Lignin historical, biological, and materials perspectives”, Eds. by W. G. Glasser, R. A. Northey, and T. P. Schultz, ACS Symposium Series, Vol. 742, American Chemical Society, 216 (1999).


R. W. Whetten, J. J. Mackay, and R. R. Sederoff, “Recent advances in understanding lignin biosynthesis”,
Annu. Rev. Plant Physiol. Plant Mol. Biol.,
49, 585 (1998).



A. Scalbert, “Ether linkage between phenolic acids and lignin fractions from wheat straw”,
Phytochem.,
24, 1359 (1985).


A. Vishtal and A. Kraslawski, “Challenges in industrial applications of technical lignins”,
Bioresources,
6, 3547 (2011).


W. O. S. Doherty, P. Mousavioun, and C. M. Fellows, “Value-adding to cellulosic ethanol: Lignin polymers”,
Ind. Crop. Prod.,
33, 259 (2011).


J. C. Carvajal, Á. Gómez, and C. A. Cardona, “Comparison of lignin extraction processes: Economic and environmental assessment”,
Bioresour. Technol.,
214, 468 (2016).



N. Mandlekar, A. Cayla, F. Rault, S. Giraud, F. Salaün, G. Malucelli, and J.-P. Guan, “
An overview on the use of lignin and its derivatives in fire retardant polymer systems”, In “
Lignin - trends and applications”, Eds. by M. Poletto, InTech, 2777 (2018).


J. H. Lora and W. G. Glasser, “Recent industrial applications of lignin: a sustainable alternative to nonrenewable materials”,
J. Polym. Environ.,
10, 39 (2002).


A. Tejado, C. Peña, J. Labidi, J. M. Echeverria, and I. Mondragon, “Physico-chemical characterization of lignins from different sources for use in phenol–formaldehyde resin synthesis”,
Bioresour. Technol.,
98, 1655 (2007).



H. Ľudmila, J. Michal, Š. Andrea, and H. Aleš, “Lignin, potential products and their market value”,
Wood Res.,
6, 973 (2015).

A. Tribot, G. Amer, M. Abdou Alio, H. de Baynast, C. Delattre, A. Pons, J.-D. Mathias, J.-M. Callois, C. Vial, P. Michaud, and C.-G. Dussap, “Wood-lignin: Supply, extraction processes and use as bio-based material”,
Eur. Polym. J.,
112, 228 (2019).


Z. Strassberger, S. Tanase, and G. Rothenberg, “The pros and cons of lignin valorisation in an integrated biorefinery”,
RSC Adv.,
4, 25310 (2014).


S. Laurichesse and L. Avérous, “Chemical modification of lignins: Towards biobased polymers”,
Prog. Polym, Sci.,
39, 1266 (2014).


H. Sixta, “Handbook of pulp”, Wiley-VCH (2006).


M. K. R. Konduri and P. Fatehi, “Production of water-soluble hardwood kraft lignin via sulfomethylation using formaldehyde and sodium sulfite”,
ACS Sustainable Chem. Eng.,
3, 1172 (2015).


A. E. Kazzaz, Z. Hosseinpour Feizi, and P. Fatehi, “Interaction of sulfomethylated lignin and aluminum oxide”,
Colloid Polym. Sci.,
296, 1867 (2018).


Y. Qin, D. Yang, W. Guo, and X. Qiu, “Investigation of grafted sulfonated alkali lignin polymer as dispersant in coal-water slurry”,
J. Ind. Eng. Chem.,
27, 192 (2015).


A. J. Ragauskas and C. G. Yoo, “Editorial: advancements in biomass recalcitrance: The use of lignin for the production of fuels and chemicals”,
Front. Energy Res.,
6, 118 (2018).


J. F. Kadla and S. Kubo, “Miscibility and hydrogen bonding in blends of poly(ethylene oxide) and kraft lignin”,
Macromolecules,
36, 7803 (2003).


Y. Cao, S. S. Chen, S. Zhang, Y. S. Ok, B. M. Matsagar, K. C.-W. Wu, and D. C. W. Tsang, “Advances in lignin valorization towards bio-based chemicals and fuels: Lignin biorefinery”,
Bioresour. Technol.,
291, 121878 (2019).



G. E. Fredheim, S. M. Braaten, and B. E. Christensen, “Molecular weight determination of lignosulfonates by size-exclusion chromatography and multi-angle laser light scattering”,
J. Chromatogr. A,
942, 191 (2002).


J. K. Sameni, “
Physico-chemical characterization of lignin isolated from industrial sources for advanced applications”, Ph.D. Dissertation, University of Toronto, Canada. (2015).

J. Lange, “Renewable feedstocks: The problem of catalyst deactivation and its mitigation”,
Angew. Chem. Int. Ed.,
54, 13186 (2015).



H. Ye, Y. Zhang, and Z. Yu, “Effect of desulfonation of lignosulfonate on the properties of poly (lactic acid)/lignin composites”,
Bioresource,
3, 4810 (2017).

T. Aro and P. Fatehi, “Production and application of lignosulfonates and sulfonated lignin”,
ChemSusChem.,
10, 1861 (2017).



P. Fatehi and J. Chen, “
Extraction of technical lignins from pulping spent liquors, challenges and opportunities”, In “
Production of biofuels and chemicals from lignin”, Eds. by Z. Fang, and R. L. Smith, Springer, 35 (2016).



D. Kun and B. Pukánszky, “Polymer/lignin blends: interactions, properties, applications,”
Eur. Polym. J.,
93, 618 (2017).


A. Berlin and M. Balakshin, “Industrial lignins: analysis, properties, and applications”, In “Bioenergy research: advances and applications”, Eds by V. K. Gupta, C. P. Kubicek, J. Saddler, F. Xu, and M. G. Tuohy, Elsevier Book Series, Elsevier, 315 (2014).



A. Shrotri, H. Kobayashi, and A. Fukuoka, “
Catalytic conversion of structural carbohydrates and lignin to chemicals”, In “
Advances in catalysis”, Eds. by M. Dieguez, Elsevier Book Series, Elsevier, 59 (2017).


J. H. Lora and W. G. Glasser, “Recent industrial applications of lignin: A sustainable alternative to nonrenewable materials”,
J. Polym. Environ.,
10, 39 (2002).


N. Smolarski, “High-value opportunities for lignin: unlocking its potential”,
Frost & Sullivan, November 07, (2012).

P. Alvira, E. Tomás-Pejó, M. Ballesteros, and M. J. Negro, “Pretreatment technologies for an efficient bioethanol production process based on enzymatic hydrolysis: A review”,
Bioresour. Technol.,
101, 4851 (2010).



Y. Sun and J. Cheng, “Hydrolysis of lignocellulosic materials for ethanol production: a review”,
Bioresour. Technol.,
83, 1 (2002).


M. N. Belgacem, A. Blayo, and A. Gandini, “Organosolv lignin as a filler in inks, varnishes and paints”,
Ind. Crop. Prod.,
18, 145 (2003).


E. Ahmad and K. K. Pant, “
Lignin conversion: A key to the concept of lignocellulosic biomass-based integrated biorefinery”, In “
Waste biorefinery”, Eds. by T. Bhaska, A. Pandey, S. V. Mohan, D.-J. Lee, and S. K. Khanal, Elsevier, 409 (2018).



D. A. Baker and T. G. Rials, “Recent advances in low-cost carbon fiber manufacture from lignin”,
J. Appl. Polym. Sci.,
130, 713 (2013).


H. Sadeghifar and D. S. Argyropoulos, “Correlations of the antioxidant properties of softwood kraft lignin fractions with the thermal stability of its blends with polyethylene”,
ACS Sustainable Chem. Eng.,
3, 349 (2015).


M. R. Snowdon, A. K. Mohanty, and M. Misra, “A study of carbonized lignin as an alternative to carbon black”,
ACS Sustainable Chem. Eng.,
2, 1257 (2014).


P. Myllytie, M. Misra, and A. K. Mohanty, “Carbonized lignin as sustainable filler in biobased poly(trimethylene terephthalate) polymer for injection molding applications”,
ACS Sustainable Chem. Eng.,
4, 102 (2016).


S. Gillet, M. Aguedo, L. Petitjean, A. R. C. Morais, A. M. da Costa Lopes, R. M. Łukasik, and P. T. Anastas, “Lignin transformations for high value applications: towards targeted modifications using green chemistry”,
Green Chem.,
19, 4200 (2017).


S. Hu, S. Zhang, N. Pan, and Y.-L. Hsieh, “High energy density supercapacitors from lignin derived submicron activated carbon fibers in aqueous electrolytes”,
J. Power Sources,
270, 106 (2014).


A. Cayla, F. Rault, S. Giraud, F. Salaün, V. Fierro, and A. Celzard, “PLA with intumescent system containing lignin and ammonium polyphosphate for flame retardant textile”,
Polymers,
9, 331 (2016).




S. R. Yearla and K. Padmasree, “Preparation and characterisation of lignin nanoparticles: evaluation of their potential as antioxidants and UV protectants”,
J. Exp. Nanosci.,
11, 289 (2015).


C. D. Scown, A. A. Gokhale, P. A. Willems, A. Horvath, and T. E. McKone, “Role of lignin in reducing life-cycle carbon emissions, water use, and cost for united states cellulosic biofuels”,
Environ. Sci. Technol.,
48, 8446 (2014).



J. E. Holladay, J. F. White, J. J. Bozell, and D. Johnson, “Top value-added chemicals from biomass; Volume II: results of screening for potential candidates from biorefinery lignin”,
Office of Scientific and Technical Information (OS-TI), (2007).


J. Jung, L. Zhang, and J. Zhang, “
Lead-acid battery technologies: fundamentals, materials, and applications”, CRC Press (2015).


S. V. Gnedenkov, D. P. Opra, L. A. Zemnukhova, S. L. Sinebryukhov, I. A. Kedrinskii, O. V. Patrusheva, A. Grossman, and V. Wilfred, “Lignin-based polymers and nanomaterials”,
Curr. Opin. Biotechnol.,
56, 112 (2018).

W. Zhang, J. Yin, Z. Lin, H. Lin, H. Lu, Y. Wang, and W. Huang, “Facile preparation of 3D hierarchical porous carbon from lignin for the anode material in lithium ion battery with high rate performance”,
Electrochim. Acta.,
176, 1136 (2015).


S. M. Fonseca, T. Moreira, A. J. Parola, C. Pinheiro, and C. A. Laia, “PEDOT electrodeposition on oriented mesoporous silica templates for electrochromic devices”,
Sol. Energy Mater. Sol. Cells,
159, 94 (2017).


T. Aso, K. Koda, S. Kubo, T. Yamada, I. Nakajima, and Y. Uraki, “Preparation of novel lignin-based cement dispersants from isolated lignins”,
J. Wood Chem. Technol.,
33, 286 (2013).


W. Z. Ouyang, Y. Huang, H. J. Luo, and D. S. Wang, “Preparation and properties of poly(lactic acid)/cellulolytic enzyme lignin/PGMA ternary blends”,
Chin. Chem. Lett.,
23, 351 (2012).


A. Kamoun, A. Jelidi, and M. Chaabouni, “Evaluation of the performance of sulfonated esparto grass lignin as a plasticizer-water reducer for cement”,
Cem. Concr. Res.,
33, 995 (2003).


J. J. Meister, “Modification of lignin”,
J. Macromol. Sci., Polym. Rev.,
42, 235 (2002).


P. Dilling, and M. S. Dimitri, U.S. patent 4,891,070 (1990).

F. G. Calvo-Flores and J. A. Dobado, “Lignin as renewable raw material”,
ChemSusChem.,
3, 1227 (2010).



T. C. Nirmale, B. B. Kale, and A. J. Varma, “A review on cellulose and lignin based binders and electrodes: Small steps towards a sustainable lithium ion battery”,
Int. J. Biol. Macromol.,
103, 1032 (2017).



A. Rangan, M. V. Manjula, K. G. Satyanarayana, and R. Menon, “
Lignin/nanolignin and their biodegradable composites,” In “
Biodegradable green composites”, John Wiley & Sons, 167-198 (2016).


P. Figueiredo, K. Lintinen, J. T. Hirvonen, M. A. Kostiainen, and H. A. Santos, “Properties and chemical modifications of lignin: Towards lignin-based nanomaterials for biomedical applications”,
Prog. Mater. Sci.,
93, 233 (2018).


P. Mishra and R. Wimmer, “Aerosol assisted self-assembly as a route to synthesize solid and hollow spherical lignin colloids and its utilization in layer by layer deposition”,
Ultrason. Sonochem.,
35, 45 (2017).



I. E. Raschip, E. G. Hitruc, and C. Vasile, “Semi-interpenetrating polymer networks containing polysaccharides. II. Xanthan/lignin networks: a spectral and thermal characterization”,
High Perform. Polym.,
23, 219 (2011).


E. Ten and W. Vermerris, “Recent developments in polymers derived from industrial lignin”,
J. Appl. Polym. Sci.,
132, 42069 (2014).


F. Zamboni, S. Vieira, R. L. Reis, J. M. Oliveira, and M. N. Collins, “The potential of hyaluronic acid in immunoprotection and immunomodulation: chemistry, processing and function”,
Prog. Mater. Sci.,
97, 97 (2018).


V. K. Thakur and M. K. Thakur, “Recent advances in green hydrogels from lignin: a review”,
Int. J. Biol. Macromol.,
72, 834 (2015).



W. K. El-Zawawy, “Preparation of hydrogel from green polymer”,
Polym. Adv. Technol.,
16, 48 (2005).


L. Passauer, K. Fischer, and F. Liebner, “Preparation and physical characterization of strongly swellable oligo (oxyethylene) lignin hydrogels”,
Holzforschung,
65, 309 (2011).


H. A. Hegazi, “Removal of heavy metals from wastewater using agricultural and industrial wastes as adsorbents”,
HBRC J.,
9, 276 (2013).


Y. Ge and Z. Li, “Application of lignin and its derivatives in adsorption of heavy metal ions in water: A review”,
ACS Sustainable Chem. Eng.,
6, 7181 (2018).


X. Guo, S. Zhang, and X. Shan, “Adsorption of metal ions on lignin”,
J. Hazard. Mater.,
151, 134 (2008).



M. A. Chowdhury, “The controlled release of bioactive compounds from lignin and lignin-based biopolymer matrices”,
Int. J. Biol. Macromol.,
65, 136 (2014).



C. Yu, F. Wang, C. Zhang, S. Fu, and L. A. Lucia, “The synthesis and absorption dynamics of a lignin-based hydrogel for remediation of cationic dye-contaminated effluent”,
React. Funct. Polym.,
106, 137 (2016).


S. S. Y. Tan, D. R. MacFarlane, J. Upfal, L. A. Edye, W. O. S. Doherty, A. F. Patti, J. M. Pringle, and J. L. Scott, “Extraction of lignin from lignocellulose at atmospheric pressure using alkylbenzenesulfonate ionic liquid”,
Green Chem.,
11, 339 (2009).


F. Flores-Céspedes, G. P. Martínez-Domínguez, M. Villafranca-Sánchez, and M. Fernández-Pérez, “Preparation and characterization of azadirachtin alginate-biosorbent based formulations: water release kinetics and photodegradation study”,
J. Agric. Food Chem.,
63, 8391 (2015).



H.-W. Kammer, “Surface and Interfacial Tension of polymer melts-thermodynamic theory of the interface between immiscible polymers”,
Zeitschrift für Physikalische Chemie,
2580, 1149 (1977).


G. I. Taylor, “The formation of emulsions in definable fields of flow”,
Proc. R. Soc. Lond., Ser. A,
146, 501 (1934).


I. Fortelný, P. Kamenická, and J. Kovář, “Effect of the viscosity of components on the phase structure and impact strength of polypropylene/ethylene-propylene elastomer blends”,
Angew. Makromol. Chem.,
164, 125 (1988).


J. Móczó, E. Fekete, and B. Pukánszky, “Acid-base interactions and interphase formation in particulate-filled polymers”,
J. Adhes.,
78, 861 (2002).


G. Szabo, V. Romhanyi, D. Kun, K. Renner, and B. Puká́nszky, “Competitive interactions in aromatic polymer/lignosulfonate blends”,
ACS Sustainable Chem. Eng.,
5, 410 (2017).


K. Choo, Y. Ching, C. Chuah, S. Julai, and N.-S. Liou, “Preparation and characterization of polyvinyl alcohol-chitosan composite films reinforced with cellulose nanofiber”,
Materials,
9, 644 (2016).




S. Suzuki, A. Ishikuro, D. Hirose, K. Ninomiya, and K. Takahashi, “Dual catalytic activity of an ionic liquid in lignin acetylation and deacetylation”,
Chem. Lett.,
47, 860 (2018).


H. Wang, W. Chen, X. Zhang, Y. Wei, A. Zhang, S. Liu, X. Wang, and C. Liu, “Structural changes of bagasse during the homogeneous esterification with maleic anhydride in ionic liquid 1-allyl-3-methylimidazolium chloride”,
Polymers10, 433 (2018).




H. Wang, X. Zhang, Y. Wei, A. Zhang, C. Liu, and R. Sun, “Homogeneous esterification mechanism of bagasse modified with phthalic anhydride in ionic liquid, part 3: structural transformation of lignins”,
Bioresources,
12, 4062 (2017).


S. Laurichesse and L. Avérous, “Synthesis, thermal properties, rheological and mechanical behaviors of lignins-grafted-poly(ε-caprolactone)”,
Polymer,
54, 3882 (2013).


H. Nagele, J. Pfitzer, E. Nagele, E. R. Inone, N. Eisenreich, W. Eckl, and P. Eyerer, “
Arboform - a thermoplastic, processable material from lignin and natural fibers”, In “C
hemical modification, properties, and usage of lignin”, Eds. by T. Q. Hu, Kluwer Academic/Plenum Publishers, pp 101 (2002).


S. Sahoo, M. Misra, and A. K. Mohanty, “Effect of compatibilizer and fillers on the properties of injection molded lignin-based hybrid green composites”,
J. Appl. Polym. Sci.,
127, 4110 (2013).


Y. Li and S. Sarkanen, “
Thermoplastics with very high lignin contents”, In “
Lignin: historical, biological, and materials perspectives”, Eds. by W. G. Glasser, R. A. Northey, and T. P. Schultz, ACS Symposium Series Vol. 742, American Chemical Society, 351 (1999).


A. Duval and M. Lawoko, “A review on lignin-based polymeric, micro- and nano-structured materials”,
React. Funct. Polym.,
85, 78 (2014).


A. Tejado, C. Pena, J. Labidi, J. M. Echeverria, and I. Mondragon, “Physico-chemical characterization of lignins from different sources for use in phenol-formaldehyde resin synthesis”,
Bioresour. Technol.,
98, 1655 (2007).



A. Lee and Y. Deng, “Green polyurethane from lignin and soybean oil through nonisocyanate reactions”,
Eur. Polym. J.,
63, 67 (2015).


C. Sasaki, M. Wanaka, H. Takagi, S. Tamura, C. Asada, and Y. Nakamura, “Evaluation of epoxy resins synthesized from steam-exploded bamboo lignin”,
Ind. Crop. Prod.,
43, 757 (2013).


C. Asada, S. Basnet, M. Otsuka, C. Sasaki, and Y. Nakamura, “Epoxy resin synthesis using low molecular weight lignin separated from various lignocellulosic materials”,
Int. J. Biol. Macromol.,
74, 413 (2015).



I. T. Kim, T. K. Sinha, J. Lee, Y. Lee, and J. S. Oh, “Ultrasonic treatment: An Acid-free green approach toward preparing high performance activated carbon from lignin”,
Ind. Eng. Chem. Res.,
60, 2439 (2021).


N. Mahmood, Z. Yuan, J. Schmidt, and C. C Xu, “Depolymerization of lignins and their applications for the preparation of polyols and rigid polyurethane foams: a review”,
Renew. Sustain. Energy Rev.,
60, 317 (2016).


H. Jeong, J. Park, S. Kim, J. Lee, and N. Ahn, “Compressive viscoelastic properties of softwood Kraft lignin-based flexible polyurethane foams”,
Fiber Polym.,
14, 1301 (2013).


R. Pucciariello, V. Villani, C. Bonini, M. D'Auria, and T. Vetere, “Physical properties of straw lignin-based polymer blends”,
Polymer,
45, 4159 (2004).


H. Jeong, J. Park, S. Kim, J. Lee, and J. W. Cho, “Use of acetylated softwood kraft lignin as filler in synthetic polymers”,
Fiber Polym.,
13, 1310 (2012).


W. G. Glasser, J. S. Knudsen, and C.-S. Chang, “Multiphase materials with lignin. III. Polyblends with ethylene-vinyl acetate copolymers”,
J. Wood Chem. Technol.,
8, 221 (1988).


F. Chen, H. Dai, X. Dong, J. Yang, and M. Zhong, “Physical properties of lignin-based polypropylene blends”,
Polym. Compos.,
32, 1019 (2011).


B. Košiková, V. Demianová, and M. Kačuráková, “Sulfur-free lignins as composites of polypropylene films”,
J. Appl. Polym. Sci.,
47, 1065 (1993).


D. Kai, K. Zhang, S. S. Liow, and X. J. Loh, “New dual functional PHB-grafted lignin copolymer: synthesis, mechanical properties, and biocompatibility studies”,
ACS Appl. Bio Mater.,
2, 127 (2018).


P. Mousavioun, W. O. S. Doherty, and G. George, “Thermal stability and miscibility of poly(hydroxybutyrate) and soda lignin blends”,
Ind. Crops Prod.32, 656 (2010).


P. Mousavioun, P. J. Halley, and W. O. S. Doherty, “Thermophysical properties and rheology of PHB/lignin blends”,
Ind. Crop. Prod.,
50, 270 (2013).


W. G. Glasser, V. Davé, and C. E. Frazier, “Molecular weight distribution of (semi-) commercial lignin derivatives”,
J. Wood Chem. Technol.,
13, 545 (1993).


K. Bahl, T. Miyoshi, and S. C. Jana, “Hybrid fillers of lignin and carbon black for lowering of viscoelastic loss in rubber compounds”,
Polymer,
55, 3825 (2014).


T. Bova, C. D. Tran, M. Y. Balakshin, J. Chen, E. A. Capanema, and A. K. Naskar, “An approach towards tailoring interfacial structures and properties of multiphase renewable thermoplastics from lignin–nitrile rubber”,
Electron. Suppl. Mater. Green Chem.,
18, 5423 (2016).


C. D. Tran, J. Chen, J. K. Keum, and A. K. Naskar, “A new class of renewable thermoplastics with extraordinary performance from nanostructured lignin-elastomers”,
Adv. Funct. Mater.,
26, 2677 (2016).


Y. Ikeda, P, Junkong, H. Yokohama, R. Kitano, T. Phakkeeree, and A. Kato, “Reinforcing biofiller “Lignin” for high performance green natural rubber nanocomposites”,
RSC Adv.,
7, 5222 (2017).


C. Miao and W. Y. Hamad, “Controlling lignin particle size for polymer blend applications”,
J. Appl. Polym. Sci.,
134, 1 (2017).


S. Laurichesse and L. Avérous, “Chemical modification of lignins: towards biobased polymers”,
Prog. Polym. Sci.,
39, 1266 (2014).


V. K. Thakur, M. K. Thakur, P. Raghavan, and M. R. Kessler, “Progress in green polymer composites from lignin for multi-functional applications: a review”,
ACS Sustainable Chem. Eng.,
2, 1072 (2014).


K. Bahl, N. Swanson, C. Pugh, and S. C. Jana, “Polybutadiene-
g-polypentafluorostyrene as a coupling agent for lignin-filled rubber compounds”,
Polymer,
55, 6754 (2014).


H. Wang, W. Liu, J. Huang, D. Yang, and X. Qiu, “Bioinspired engineering towards tailoring advanced lignin/rubber elastomers”,
Polymers,
10, 1033 (2018).




D. K. Setua, M. K. Shukla, V. Nigam, H. Singh, and G. N. Mathur, “Lignin-reinforced rubber composites”,
Polym. Compos.,
21, 988 (2000).


P. Frigerio, L. Zoia, M. Orlandi, T. Hanel, and L. Castellani, “Application of sulphur-free lignins as a filler for elastomers: effect of hexamethylenetetramine treatment”,
Bioresources,
9, 1387 (2014).


C. Jiang, H. He, X. Yao, P. Yu, L. Zhou, and D. Jia, “In situ dispersion and compatibilization of lignin/epoxidized natural rubber composites: Reactivity, morphology and property”,
J. Appl. Polym. Sci.,
132, 1 (2015).


K. Bahl and S. C. Jana, “Surface modificationof lignosulfonates for reinforcement of styrene-butadiene rubber compounds”,
J. Appl. Polym. Sci.,
131, 1 (2014).


H. Wang, W. Liu, J. Huang, D. Yang, and X. Qiu, “Bioinspired engineering towards tailoring advanced lignin/rubberelastomers”,
Polymers,
10, 1033 (2018).




J.-Y. Sun, X. Zhao, W. R. K. Illeperuma, O. Chaudhuri, K. H. Oh, D. J. Mooney, J. J. Vlassak, and Z. Suo, “Highly stretchable and tough hydrogels”,
Nature,
489, 133 (2012).




C. N. Z. Schmitt, Y. Politi, A. Reinecke, and M. J. Harrington, “Role of sacrificial protein-metal bond exchange inmussel byssal thread self-healing”,
Biomacromolecules,
16, 2852 (2015).



H. J. Zhang, T. L. Sun, A. K. Zhang, Y. Ikura, T. Nakajima, T. Nonoyama, T. Kurokawa, O. Ito, H. Ishitobi, and J. P. Gong, “Tough physical double-network hydrogels based on amphiphilic triblock copolymers”,
Adv. Mater.,
28, 4884 (2016).



C. Jiang, H. He, H. Jiang, L. Ma, and D. M. Jia, “Nano-lignin filled natural rubber composites: preparation and characterization”,
Express Polym. Lett.,
7, 480 (2013).


F. Bertini, M. Canetti, A. Cacciamani, G. Elegir, M. Orlandi, and L. Zoia, “Effect of ligno-derivatives on thermal properties and degradation behavior of poly(3-hydroxybutyrate)-based biocomposites”,
Polym. Degrad. Stab.,
97, 1979 (2012).


D. Barana, S. D. Ali, A. Salanti, M. Orlandi, L. Castellani, T. Hanel, and L. Zoia, “Influence of lignin features on thermal stability and mechanical properties of natural rubber compounds”,
ACS Sustainable Chem. Eng.,
4, 5258 (2016).